登录/
注册
登录/
注册
卡比马唑
Kabimazuo
Carbimazole
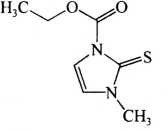
C7H10N2O2S 186.23
本品为3-甲基-2-硫代咪唑啉-1-羧酸乙酯。按干燥品计算,含C7H10N2O2S不得少于98.5%。
本品为白色或类白色的结晶性粉末;有特臭。
本品在三氯甲烷中易溶,在乙醇中略溶,在水或乙醚中微溶。
熔点本品的熔点(通则0612)为122~125℃。
用于甲状腺功能亢进症,包括Graves病(伴自身免疫功能紊乱、甲状腺弥散性肿大,可有突眼)、甲状腺腺瘤、结节性甲状腺肿及甲状腺癌所引起者。在Graves病中,尤其适用于:①病情较轻,甲状腺轻至中度肿大患者。②青少年及儿童、老年患者。③甲状腺手术后复发,又不适于用放射性131I治疗者。④手术前准备。⑤作为131I放疗的辅助治疗。现已较少应用。
口服 成人开始剂量一般一日30mg,视病情轻重调整为一日15~40mg,分次口服,病情控制后逐渐减量。维持量按病情需要一日5~15mg,疗程一般12~18个月。
【儿科用法与用量】口服开始时用量按体重0.4mg/(kg·d),分次口服。维持量约减半,按病情决定。
甲巯咪唑的前体——卡比马唑在体内快速转换为甲巯咪唑(10mg的卡比马唑转换成6mg的甲巯咪唑),甲巯咪唑和卡比马唑的作用方式是相同的。本品在体内逐渐水解成甲巯咪唑后发挥作用,故作用缓慢,疗效维持时间较长。
美国FDA妊娠期用药安全性分级为口服给药D。
卡比马唑片:5mg。
(1)取本品10mg,加水5ml,加热使溶解,放冷,加稀碘化铋钾试液1ml,即生成猩红色沉淀。
(2)取含量测定项下的溶液,照紫外-可见分光光度法(通则0401)测定,在227nm与292nm的波长处有最大吸收。
(3)本品的红外光吸收图谱应与对照的图谱(光谱集95图)一致。
甲巯咪唑照薄层色谱法(通则0502)试验。
供试品溶液 取本品适量,精密称定,加三氯甲烷溶解并稀释制成每1ml中约含10mg的溶液。
对照品溶液 取甲巯咪唑对照品适量,精密称定,加三氯甲烷溶解并定量稀释制成每1ml中约含50μg的溶液。
色谱条件 采用硅胶G薄层板,以三氯甲烷-丙酮(4:1)为展开剂。
测定法 吸取供试品溶液与对照品溶液各10μl,分别点于同一薄层板上,展开,晾干,喷以稀碘化铋钾试液使显色。
限度 供试品溶液如显与对照品溶液相应的杂质斑点,其颜色与对照品溶液的主斑点比较,不得更深(0.5%)。
干燥失重 取本品,在80℃干燥至恒重,减失重量不得过0.5%(通则0831)。
炽灼残渣 不得过0.1%(通则0841)。
照紫外-可见分光光度法(通则0401)测定。
供试品溶液 取本品约50mg,精密称定,置500ml量瓶中,加水使溶解并稀释至刻度,摇匀,精密量取10ml,置100ml量瓶中,加盐酸溶液(9→100)10ml,用水稀释至刻度,摇匀。
测定法 取供试品溶液,在292nm的波长处测定吸光度,按C7H10N2O2S的吸收系数(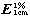 )为557计算。
)为557计算。
抗甲状腺药。
密封保存。
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
