登录/
注册
登录/
注册
胰激肽原酶
Yijitaiyuanmei
PancreaticKininogenase
本品系自猪胰中提取的蛋白酶。每1mg蛋白含胰激肽原酶的活力不得少于300单位(供口服用)或600单位(供注射用)。
本品应从检疫合格的猪胰中提取,生产过程应符合现行版《药品生产质量管理规范》的要求。本品来源于动物,在生产过程中应采用适宜的病毒灭活工艺等方法进行病毒安全性控制。
本品为白色或类白色粉末;无臭。
本品在水中易溶,在乙醇或乙醚中几乎不溶。
血管扩张药,有改善微循环作用。主要用于微循环障碍性疾病,如糖尿病引起的肾病、周围神经病、视网膜病变、眼底病变及缺血性脑血管病,也可用于高血压病的辅助治疗。
(1)口服一日3次,一次120~240U,空腹服用。
(2)肌内注射临用前以注射用水或注射用灭菌0.9%氯化钠注射液1.5ml溶解。一日1次或隔日1次,一次10~40U,可根据年龄、症状适当增减用量。
胰激肽原酶能提高机体内激肽系统活性,释放缓激肽。缓激肽作用于血管平滑肌,使小血管和毛细血管扩张,增加毛细血管通透性和血流量,改善微循环。胰激肽原酶作为活化因子能激活纤溶系统,降低血液黏度以防止血栓形成,改善各器官血流。胰激肽原酶通过缓激肽激活磷脂酶A₂,增加花生四烯酸的合成,进而合成内源性PG,增加肾血流量,改善肾功能,减少尿蛋白。胰激肽原酶能降低外周阻力,促进水、钠排泄,具有降压作用。
偶有皮疹、皮肤瘙痒等过敏现象及胃部不适和倦怠等感觉,停药后即消失。因注射给药偶会引起休克,使用时应充分观察,发现异常立即终止给药并进行适当处置。
(1)脑出血及其他出血性疾病的急性期禁用。
(2)对本品过敏患者禁止注射给药。
(3)本品注射剂型内含有苯甲醇,禁止用于儿童肌内注射。
(1)本品用药前请详询过敏史。
(2)本品注射剂型仅供肌内注射给药。
(3)本品口服剂型为肠溶衣片,应整片吞服以防药物在胃中被破坏。
(4)过敏性体质患者注射给药后须观察15~20分钟。
(5)注射过程中须备有肾上腺素水针、氧气和可以静脉注射的皮质类固醇等应急抢救药品。
(1)胰激肽原酶与胰蛋白酶抑制药不能同时使用。
(2)胰激肽原酶与血管紧张素转使酶抑制药(ACED有协同作用。
胰激肽原酶片:(1)60U;(2)120U;(3)240U。
胰激肽原酶针剂:(1)10U;(2)40U。
(1)照紫外-可见分光光度法(通则0401)测定。
供试品溶液取已测得效价的本品适量,精密称定,加纯度项下的磷酸盐缓冲液(pH7.0)溶解并定量稀释制成每1ml中含10单位的溶液。精密量取4ml,置10ml量瓶中,用上述磷酸盐缓冲液(pH7.0)稀释至刻度。
测定法取效价测定酶活力项下的底物溶液2.9ml,在30℃±0.5℃预热5分钟,置1cm比色池中,精密加入供试品溶液0.1ml,混匀,立即计时,使比色池内的温度保持在30℃±0.5℃,在253nm的波长处测定,以上述磷酸盐缓冲液(pH7.0)0.1ml代替供试品溶液,同法操作,作为空白对照。准确读取4分钟时的吸光度(A4)和6分钟时的吸光度(A6)。求得A值[(A6-A4/2],按下式计算。
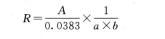
式中a为供试品溶液每1ml中的毫克数;
b为供试品每1mg的效价单位数。
结果判定R值(水解速率)应为0.12~0.17。
(2)在纯度项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
酸碱度 取本品适量,加水溶解并稀释制成每1ml中含300单位的溶液,依法测定(通则0631),pH值应为5.5~7.5。
溶液的澄清度 取本品适量,加水溶解并稀释制成每1ml中含2mg的溶液,依法检查(通则0902第一法),溶液应澄清。(供注射用)
脂肪 取本品1.0g,置具塞锥形瓶中,加乙醚20ml,密塞,时时旋动,放置约30分钟后,将乙醚液倾至用乙醚润湿的滤纸上,滤过,再用乙醚10ml洗涤残渣,合并滤液及洗液至已恒重的蒸发皿中,除去乙醚,在105℃干燥2小时,精密称定,遗留脂肪不得过5mg。
相关蛋白酶照紫外-可见分光光度法(通则0401)测定。
供试品溶液 取本品适量,加纯度项下的磷酸盐缓冲液(pH7.0)溶解并稀释制成每1ml中含1单位的溶液。
测定法 精密量取供试品溶液1ml置试管中,在35℃±0.5℃水浴中保温5分钟,精密加入已预热至35℃±0.5℃的酪蛋白溶液(取酪蛋白0.6g,加0.05mol/L磷酸氢二钠溶液80ml,65℃加热溶解,放冷,调节pH值至8.0,用水稀释至100ml,临用前配制)5ml,混匀,于35℃±0.5℃水浴中准确反应20分钟,再精密加入5%三氯醋酸溶液5ml,混匀,滤过,取续滤液作为测定溶液;另精密量取供试品溶液1ml,置试管中,精密加入5%三氯醋酸溶液5ml,混匀,于35℃±0.5℃水浴中准确反应20分钟,再精密加入上述酪蛋白溶液5ml,混匀,滤过,取续滤液作为空白,在2小时内,在280nm的波长处分别测定吸光度。
限度吸光度 不得过0.2。
纯度照高效液相色谱法(通则0512)测定。
磷酸盐缓冲液(pH7.0)取磷酸氢二钠10.9g,磷酸二氢钠2.3g,加水溶解并稀释至1000ml,用50%磷酸溶液调节pH值至7.0。
供试品溶液 取本品适量,加流动相A溶解并稀释制成每1ml中约含200单位的溶液。
对照品溶液 取胰激肽原酶对照品(纯度应大于95%)适量,加流动相A溶解并定量稀释制成每1ml中约含200单位的溶液。
色谱条件 用疏水性凝胶为填充剂(TSKgelPhenyl-5PW,7.5mm×75mm,10μm或其他适宜的色谱柱);以含1.7mol/L硫酸铵的磷酸盐缓冲液(pH7.0)为流动相A,以磷酸盐缓冲液(pH7.0)为流动相B,按下表进行梯度洗脱;柱温为25℃;流速为每分钟0.5ml;检测波长为280nm;进样体积20μl。

系统适用性 要求理论板数按胰激肽原酶峰计算不低于1500,胰激肽原酶主峰与相邻杂质峰之间的分离度不得低于0.8。
测定法 精密量取流动相A、供试品溶液与对照品溶液,分别注入液相色谱仪,记录色谱图。将供试品溶液与对照品溶液的色谱图扣除流动相A色谱图(作为空白基线),进行基线校正。
限度 供试品溶液色谱图中,量取空白基线拐点(约16分钟)后所有色谱峰面积,按面积归一化法计算,与对照品溶液主峰保留时间一致的主峰面积不得低于75%(供口服用)或90%(供注射用)。
干燥失重 取本品0.50g,以五氧化二磷为干燥剂,在60℃减压干燥4小时,减失重量不得过5.0%(通则0831)。
炽灼残渣 取本品0.50g,依法检查(通则0841),遗留残渣不得过3.0%。
细菌内毒素 取本品,依法检查(通则1143),每1单位胰激肽原酶中含内毒素的量应小于2.5EU。(供注射用)
血管舒张药。
遮光,密封,在阴凉干燥处保存。
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
