登录/
注册
登录/
注册
头孢地嗪钠
Toubaodiqinna
CefodizimeSodium
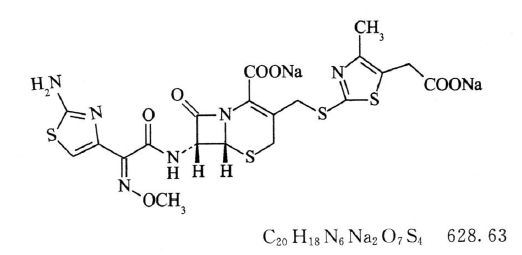
本品为(6R,7R)-7-[(Z)-2-(2-氨基噻唑-4-基)-2-(甲氧亚氨基)乙酰氨基]-3-[(5-羧甲基-4-甲基噻唑-2-基)硫甲基]-8-氧代-5-硫杂-1-氮杂双环[4.2.0]辛-2-烯-2-甲酸二钠盐。按无水、无乙醇物计算,含C20H20N6O7S4不得少于88.0%。
本品为白色至微黄色的粉末或结晶性粉末;无臭或稍有特异性气味。
本品在水中极易溶解,在无水乙醇或乙醚中几乎不溶。
比旋度取本品,精密称定,加水溶解并定量稀释制成每1ml中约含10mg的溶液,依法测定(通则0621),比旋度为-55°至-62°。
吸收系数取本品,精密称定,加水溶解并定量稀释制成每1ml中约含20μg的溶液,照紫外-可见分光光度法(通则0401),在260nm波长处测定吸光度,吸收系数(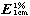 )为305~3350
)为305~3350
适用于敏感菌所致下呼吸道感染、尿路感染、脑膜炎、妇科感染、外科感染等;亦可用于淋菌性尿道炎等。由于本品对机体免疫功能有增强作用,尤其适用于老年人、糖尿病患者或慢性尿毒症等免疫缺陷患者感染的治疗。
(1)成人每日2~4g,分1~2次静脉注射、静脉滴注或肌内注射给药。单纯性下尿路感染,1~2g单剂给药。单纯性淋病奈瑟菌感染,0.25~1g单剂给药。
(2)肾功能不全患者需调整给药剂量:肌酐清除率为10~30ml/min者,每日最大剂量为2g;肌酐清除率<10ml/min者,上述剂量减半;血液透析患者,于透析后给药1~2g。
(1)药效学 本品对革兰阳性菌及革兰阴性菌具有广谱抗菌作用。甲氧西林敏感金黄色葡萄球菌对本品敏感,表皮葡萄球菌、甲氧西林耐药金黄色葡萄球菌、肠球菌属和单核细胞增多性李斯特菌对本品耐药。肺炎链球菌、化脓性链球菌、无乳链球菌及其他链球菌均对本品敏感。其抗菌活性与第一代及第二代头孢菌素相仿。肠杆菌科细菌中的大肠埃希菌、肺炎克雷伯菌、摩氏摩根菌、奇异变形菌、普通变形菌、宋内志贺菌、小肠结肠炎耶尔森菌及沙门菌属等对本品高度敏感。本品对柠檬酸杆菌、黏质沙雷菌作用较差,对肠杆菌属、不动杆菌属、铜绿假单胞菌及嗜麦芽窄食单胞菌无抗菌活性。本品对氨苄西林敏感及耐药流感嗜血杆菌、卡他莫拉菌、产β内酰胺酶及非产β内酰胺酶淋病奈瑟菌及脑膜炎奈瑟菌具有高度抗菌活性。
头孢地嗪钠对机体参与免疫功能的多形核细胞、单核细胞、巨噬细胞和淋巴细胞均有刺激作用,该作用有利于治疗免疫功能低下者的感染。头孢地嗪可增强多形核细胞、巨噬细胞及淋巴细胞的活性;对正常人及吞噬功能减退患者均可增强其吞噬细胞的趋化、吞噬及杀菌功能,提高CD4+淋巴细胞数,使CD4+/CD8+比例增高或恢复正常,刺激淋巴细胞增生、分化。本品的体内抗菌活性较体外抗菌作用显著为强。本品可刺激宿主细胞因子分泌增多,从而使免疫系统各个细胞成分的作用协同加强。
(2)药动学 静脉注射头孢地嗪钠1g或2g后的Cmax分别为215mg/L和394mg/L:静脉滴注1g后的Cmax为124.1mg/L。本品肌内注射后的生物利用度可达90%~100%,单次肌内注射1g、2g后的tmax为1~1.5小时,Cmax分别为59.6~75.2mg/L和135mg/L。t1/2约为2.5小时,本品在老年患者和肾功能减退者的t1/2可延长。血浆蛋白结合率约为81%。体内分布广泛,用治疗剂量后2~3小时在肺组织、支气管分泌物、胸水、扁桃体、肝组织、胆囊、女性生殖系统、前列腺、肾组织和尿液中均可达到有效治疗浓度。本品可透过胎盘屏障。主要经肾小球滤过排泄,少部分经肾小管分泌,给药量的70%~80%于48小时内以原形自尿中排出。合用丙磺舒可使其尿排泄药量减少30%。持续性腹膜透析患者本品t1/2延长,血液透析可清除本品。本品在体内不被代谢。
本品耐受性良好,不良反应少见而轻微,发生率为1.2%~3.1%。因不良反应中止治疗者仅占0.9%。最常见的不良反应为肌内注射部位疼痛及静脉注射部位静脉炎等局部刺激症状,味觉障碍、腹泻、恶心、呕吐等胃肠道反应和皮疹、瘙痒等过敏反应等。其他少见不良反应有眩晕、寒战、头痛、血小板减少症、贫血等。少数患者可发生血清氨基转移酶、乳酸脱氢酶和血胆红素等升高以及生殖系统念珠菌病等。
对本品及头孢菌素类过敏者禁用。
(1)对青霉素或其他药物过敏的患者慎用本品,有青霉素过敏性休克史者避免应用,因可能与本品有交叉过敏反应。
(2)动物实验显示本品对胎儿无影响,但在妊娠期妇女中用药缺乏恰当而设计良好的对照试验。由于动物实验并不能完全预测人类反应,因此妊娠期妇女仅限于有明确指征时方可应用。
(3)哺乳期妇女应用本品宜停止授乳。
(4)不推荐本品用于儿童患者。
(1)与丙磺舒合用可延缓本品的排泄。
(2)本品与氨基糖苷类、两性霉素B、环孢素、顺铂、万古霉素、多黏菌素或黏菌素合用时,可能增强上述药物的肾毒性,应密切监测肾功能。
(3)使用强效利尿药及大剂量头孢菌素可能引起肾功能损害。
(4)本品可引起尿糖试验呈假阳性反应。
注射用头孢地嗪钠(按头孢地嗪计);(1)0.25g;(2)0.5g;(3)1g;(4)1.5g;(5)2g。
(1)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(2)本品的红外光吸收图谱应与对照的图谱(光谱集922图)一致。
(3)本品显钠盐鉴别(1)的反应(通则0301)。
酸碱度 取本品,加水制成每1ml中含0.1g的溶液,依法测定(通则0631),pH值应为5.5~7.5。
溶液的澄清度与颜色 取本品5份,分别加水制成每1ml中含头孢地嗪0.1g的溶液,溶液应澄清无色;如显浑浊,与1号浊度标准液(通则0902第一法)比较,均不得更浓;如显色,与黄色或黄绿色9号标准比色液(通则0901第一法)比较,均不得更深。
有关物质I照高效液相色谱法(通则0512)测定。临用新制。
供试品溶液 取本品约25mg,置50ml量瓶中,加流动相溶解并稀释至刻度,摇匀。
对照溶液 精密量取供试品溶液1ml,置100ml量瓶中,用流动相稀释至刻度,摇匀。
系统适用性溶液 取头孢地嗪对照品适量,加水溶解并稀释制成每1ml中约含0.1mg的溶液,取10ml,加0.1mol/L盐酸溶液1ml,室温放置24小时,再加0.1mol/L氢氧化钠溶液1ml,摇匀。
色谱条件用十八烷基硅烷键合硅胶为填充剂;以磷酸盐缓冲液(取磷酸二氢钾0.87g与无水磷酸氢二钠0.22g,加水溶解并稀释至1000ml,摇匀)-乙腈(920∶80)为流动相;检测波长为215nm;进样体积20μl。
系统适用性 要求系统适用性溶液色谱图中,头孢地嗪峰与前、后相邻的降解杂质峰之间的分离度应分别大于3.0和4.0。
测定法 精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的6倍。
限度 供试品溶液色谱图中如有杂质峰,单个杂质峰面积不得大于对照溶液主峰面积(1.0%),各杂质峰面积的和不得大于对照溶液主峰面积的1.5倍(1.5%)。
有关物质Ⅱ照分子排阻色谱法(通则0514)测定。临用新制。
供试品溶液 取本品适量,精密称定,加水溶解并定量稀释制成每1ml中含头孢地嗪0.5mg的溶液。
对照品溶液 取头孢地嗪对照品适量,精密称定,加水溶解并定量稀释制成每1ml中约含头孢地嗪5μg的溶液。
系统适用性溶液 取供试品溶液10ml,加0.1mol/L氢氧化钠溶液1ml,室温放置10分钟,再加0.1mol/L盐酸溶液lml,摇匀。
色谱条件用球状亲水硅胶(分子量适用范围为1000~10000)为填充剂;以磷酸盐缓冲液(pH7.0)[0.005mol/L磷酸氢二钠溶液-0.005mol/L磷酸二氢钠溶液(61∶39)]-乙腈(95∶5)为流动相;流速为每分钟0.8ml;检测波长为231nm;进样体积20μl。
系统适用性要求系统适用性溶液色谱图中,头孢地嗪峰与其前相邻降解杂质峰之间的分离度应符合要求。
测定法 精密量取供试品溶液与对照品溶液,分别注入液相色谱仪,记录色谱图。
限度 供试品溶液色谱图中如有杂质峰,按外标法以头孢地嗪峰计算,保留时间小于头孢地嗪的杂质的总量不得过1.5%。
残留溶剂照残留溶剂测定法(通则0861第一法)测定。
内标溶液 取正丙醇适量,用水稀释制成每1ml中含1mg的溶液。
供试品溶液 取本品约0.2g,精密称定,置顶空瓶中,精密加入内标溶液2ml使溶解,密封。
对照品溶液 分别精密称取二氯甲烷60mg、乙腈41mg和乙醇约2.0g,置50ml量瓶中,用内标溶液稀释至刻度,摇匀,精密量取5ml,置100ml量瓶中,用内标溶液稀释至刻度,摇匀,精密量取2ml,置顶空瓶中,密封。
色谱条件 以聚乙二醇(PEG-20M)(或极性相近)为固定液的毛细管柱为色谱柱;柱温为40℃;检测器温度为250℃;进样口温度为200℃;顶空瓶平衡温度为60℃,平衡时间为30分钟。
系统适用性要求对照品溶液色谱图中,各色谱峰之间的分离度均应符合要求。
测定法 取供试品溶液与对照品溶液分别顶空进样,记录色谱图。
限度 按内标法以峰面积比值计算,乙醇的残留量不得过2.0%;乙腈、二氯甲烷的残留量均应符合规定。
2-乙基己酸 取本品适量,依法测定(通则0873),不得过0.5%。
水分 取本品,照水分测定法(通则0832第一法1)测定,含水分不得过4.0%。
重金属 取本品1.0g,依法检查(通则0821第二法),含重金属不得过百万分之二十。
可见异物 取本品5份,每份2.0g,分别加微粒检查用水溶解,依法检查(通则0904),均应符合规定。(供无菌分装用)
不溶性微粒 取本品,加微粒检查用水溶解并制成每1ml中含30mg的溶液,放置10分钟,依法检查(通则0903),每1g样品中含10μm及10μm以上的微粒不得过6000个,含25μm及25μm以上的微粒不得过600个。(供无菌分装用)
细菌内毒素 取本品,依法检查(通则1143),每1mg头孢地嗪中含内毒素的量应小于0.10EU。(供注射用)
无菌 取本品,用适宜溶剂溶解并稀释后,经薄膜过滤法处理,依法检查(通则1101),应符合规定。(供无菌分装用)
照高效液相色谱法(通则0512)测定。
供试品溶液 取本品适量,精密称定,加水溶解并定量稀释制成每1ml中约含头孢地嗪0.1mg的溶液,摇匀。
对照品溶液 取头孢地嗪对照品适量,精密称定,加水溶解并定量稀释制成每1ml中约含头孢地嗪0.1mg的溶液,摇匀。
色谱条件见有关物质I项下。检测波长为262nm。
系统适用性溶液与系统适用性要求见有关物质I项下。
测定法 精密量取供试品溶液与对照品溶液,分别注入液相色谱仪,记录色谱图。按外标法以峰面积计算供试品中C20H20N6O7S4的含量。
β-内酰胺类抗生素,头孢菌素类。
密封,在凉暗干燥处保存。
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
