登录/
注册
登录/
注册
盐酸乙胺丁醇
YansuanYi’andingchun
EthambutolHydrochloride
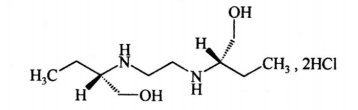
C10H24N2O2•2HCl 277.23
本品为[2R,2[S-(R*,R*)]-R]-(+)2,2'-(1,2-乙二基二亚氨基)-双-1-丁醇二盐酸盐。按干燥品计算,含C10H24N2O2•2HCl不得少于98.5%。
本品为白色结晶性粉末;无臭或几乎无臭;略有引湿性。
本品在水中极易溶解,在乙醇中略溶,在三氯甲烷中极微溶解,在乙醚中几乎不溶。
比旋度 取本品适量,精密称定,加水溶解并定量稀释制成每1ml中约含0.10g的溶液。在25℃时,依法测定(通则0621),比旋度为+6.0°至+7.0°。
适用于与其他抗结核药联合治疗结核分枝杆菌所致各型结核病,亦可用于非结核分枝杆菌感染的治疗。
成人常用量与其他抗结核药合用。①结核初治,按体重15mg/kg,一日一次性顿服;或一次口服25mg/kg,最高一日1.25g,每周2~3次。②结核复治,按体重25mg/kg,一日一次性顿服,最高一日1.25g.连续2~3个月;继以按体重15mg/kg,一日一次性顿服。③非结核分枝杆菌感染,一日15~25mg/kg,一次性顿服,亦需与其他抗结核药合用。
【儿科用法与用量】儿童常用量13岁以上儿童用量,与成人相同;13岁以下儿童用量,每日15mg/kg.但一般不作推荐。
【儿科注意事项】(1)本品有左旋、右旋、消旋异构体三种,以右旋体抗结核作用最强。
(2)常应用于结核病及其他分枝杆菌的联合治疗。
(3)不良反应多见视物模糊、红绿色盲,少数有皮疹、关节痛等过敏反应。
(1)药效学 本品为合成抑菌抗结核药。其作用机制尚未完全阐明。本品可渗入分枝杆菌体内干扰RNA的合成,从而抑制细菌的繁殖,本品只对生长繁殖期的分枝杆菌有效。单独应用时结核分枝杆菌易对本品产生耐药性;迄今未发现本品与其他抗结核药物有交叉耐药性。
(2)药动学 口服给药量的75%~80%从胃肠道吸收,tmax为2~4小时;单次口服25mg/kg,Cmax为5mg/L。广泛分布于全身各组织和体液中(除脑脊液外)。红细胞内药物浓度与血药浓度相等或为后者的2倍,并可持续24小时;肾、肺、唾液和尿液内的药物浓度都很高,但胸水和腹水中的浓度则很低。本品不能渗入正常脑膜,但结核性脑膜炎患者脑脊液中可有微量;可通过胎盘屏障进入胎儿血液循环;可从乳汁分泌,乳汁中的药物浓度约相当于母体血药浓度。其分布容积为1.6L/kg。血浆蛋白结合率为20%~30%。主要经肝脏代谢,约15%的给药量被代谢成为无活性代谢产物。经肾小球滤过和肾小管分泌排出,给药后约80%在24小时内排出,至少50%以原形排泄,约15%为无活性代谢产物。在粪便中以原形排出约20%。t1/2为3~4小时,肾功能减退者可延长至8小时。相当量的乙胺丁醇可经血液透析和腹膜透析从体内清除。
(1)发生较多者视物模糊、眼痛、红绿色盲或视力减退、视野缩小(视神经炎,每日按体重25mg/kg以上时易发生)。视力变化可为单侧或双侧,因此检查时应左眼、右眼分开测试。另有恶心、呕吐、躁狂等。
(2)发生较少者畏寒;关节肿痛(尤其是第一跖趾、踝、膝关节),病变关节表面皮肤发热并有紧绷感(急性痛风、高尿酸血症)。
(3)发生极少者为皮疹、发热等过敏反应;或麻木感、针刺感、烧灼痛或手足软弱无力(周围神经炎)。另有失明、中性粒细胞减少、血小板减少、过敏样反应等严重不良反应。
(1)对本品过敏者禁用。
(2)已报告药品对视力的不良反应或发生不能解释的视力变化者禁用。
(1)乙胺丁醇可分泌至乳汁,乳汁中的药物浓度与血药浓度相近,虽然在人类中未证实有问题,但哺乳期妇女用药需权衡利弊后再决定用药与否。
(2)对诊断的干扰服用本品可使血尿酸浓度测定值增高。
(3)痛风、视神经炎、肾功能减退者慎用。
(4)治疗期间应检查:①眼部,视野、视力、红绿色觉鉴别力等,在用药前、疗程中每日检查1次,尤其是疗程长或每日剂量超过15mg/kg的患者;②由于本品可使血清尿酸浓度增高,引起痛风发作,因此在疗程中应定期测定血清尿酸值。
(5)13岁以下儿童尚缺乏临床资料,由于在幼儿中不易监测视力变化,故本品不推荐用于13岁以下儿童。老年人往往伴有生理性肾功能减退,故应按肾功能情况调整用量。
(6)有HIV感染者或艾滋病患者需延长疗程或无限期用药。鉴于目前尚无切实可行的测定血药浓度方法,剂量应根据患者体重计算。
(7)肝或肾功能减退患者,本品血药浓度可能增高,消除半衰期延长。肾功能减退患者应用本品时需减量。
(8)美国FDA妊娠期用药安全性分级为口服给药B。
(1)与乙硫异烟胺合用可增加不良反应。
(2)与氯氧化铝合用能减少乙胺丁醇的吸收。
(3)与可能引起神经系统不良反应的药物合用可增加本品神经毒性,如视神经炎或周围神经炎。
盐酸乙胺丁醇片:0.25g。
盐酸乙胺丁醇胶囊:0.25g。
乙胺吡嗪利福异烟片(Ⅱ):每片含利福平0.15g,异烟肼0.075g,吡嗪酰胺0.4g,盐酸乙胺丁醇0.275g。
乙胺利福异烟片:每片含利福平0.12g,异烟肼0.12g,盐酸乙胺丁醇0.25g。
(1)取本品约20mg,加水2ml溶解后,加硫酸铜试液2~3滴,摇匀,再加氢氧化钠试液2~3滴,显深蓝色。
(2)本品的红外光吸收图谱应与对照的图谱(光谱集311图)一致。
(3)本品显氯化物的鉴别反应(通则0301)。
酸度 取本品适量,加水制成每1ml中含50mg的溶液,依法测定(通则0631),pH值应为3.4~4.0。
(+)2-氨基丁醇(杂质I)照薄层色谱法(通则0502)试验。
供试品溶液 取本品适量,精密称定,加甲醇溶解并定量稀释制成每1ml中约含50mg的溶液。
对照品溶液 取杂质I对照品适量,精密称定,加甲醇溶解并定量稀释制成每1ml中约含0.5mg的溶液。
系统适用性溶液 取盐酸乙胺丁醇对照品与杂质I对照品适量,加甲醇溶解并稀释制成每1ml中约含盐酸乙胺丁醇5mg与杂质I0.5mg的混合溶液。
色谱条件釆用硅胶G薄层板,以甲醇-水-浓氨溶液(75∶15∶10)为展开剂。
系统适用性要求在系统适用性溶液色谱图中应显两个清晰分离的斑点。
测定法 吸取上述三种溶液各2μl,分别点于同一薄层板上,展开,取出,晾干,于110℃加热10分钟,放冷,喷以茚三酮溶液(取茚三酮1.0g,加乙醇50ml使溶解,再加入冰醋酸10ml,摇匀),在110℃加热5分钟。
限度 供试品溶液如显与对照品溶液相应的杂质斑点,其颜色与对照品溶液的主斑点比较,不得更深(1.0%)。
有关物质照高效液相色谱法(通则0512)测定。临用新制。
供试品溶液 取本品约20mg,精密称定,置20ml量瓶中,加乙腈约10ml、三乙胺0.5ml,超声5分钟使溶解,用乙腈稀释至刻度,摇匀,精密量取4ml,置10ml量瓶中,精密加入(R)-(+)-α-甲基苄基异氰酸酯15μl,密塞,摇匀,置70℃水浴保温20分钟,放冷,摇匀。
对照溶液 精密量取供试品溶液1ml,置200ml量瓶中,用乙腈稀释至刻度,摇匀。
系统适用性溶液 取乙胺丁醇系统适用性对照品约4mg,精密称定,置10ml量瓶中,精密加入乙腈4ml和三乙胺0.1ml,超声5分钟使溶解,精密加入(R)-(+)-α-甲基苄基异氰酸酯15μl,置70℃水浴保温20分钟,放冷,摇匀。
色谱条件 用十八烷基硅烷键合硅胶为填充剂;流动相A为甲醇-水(50∶50),流动相B为甲醇,按下表进行线性梯度洗脱;检测波长为215nm;柱温为40℃;进样体积10μl。

系统适用性 要求系统适用性溶液色谱图中,乙胺丁醇衍生物峰的保留时间约为14分钟,乙胺丁醇衍生物峰与相对保留时间约为1.3处的杂质II衍生物峰之间的分离度应大于4.0。
测定法 精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图。
限度 供试品溶液色谱图中,在相对乙胺丁醇衍生物保留时间0.75~1.5之间如有杂质峰,杂质II衍生物峰面积不得大于对照溶液主峰面积的2倍(1.0%),其他单个杂质峰面积不得大于对照溶液主峰面积的0.2倍(0.1%),各杂质峰面积的和不得大于对照溶液主峰面积的2倍(1.0%),小于对照溶液主峰面积0.1倍的杂质峰可忽略不计。
干燥失重 取本品,在105℃干燥至恒重,减失重量不得过0.5%(通则0831)。
炽灼残渣 不得过0.1%(通则0841)。
重金属 取本品1.0g,加醋酸盐缓冲液(pH3.5)2ml与水适量使溶解成25ml,依法检查(通则0821第一法),含重金属不得过百万分之十。
取本品约0.2g,精密称定,置50ml量瓶中,加水20ml使溶解,加硫酸铜试液1.8ml,边振摇边加入氢氧化钠试液7ml,用水稀释至刻度,摇匀,离心(每分钟4500转),精密量取上清液10ml,加氨-氯化铵缓冲液(pH10.0)(取氯化铵70g,加水300ml溶解后,加浓氨溶液100ml,再加水稀释至1000ml,用浓氨溶液调节pH值至10.0)10ml与水100ml,加Cu-PAN试液0.15ml,用乙二胺四醋酸二钠滴定液(0.01mol/L)滴定至溶液由蓝紫色经浅红色至浅黄色,并将滴定的结果用空白试验校正。每1ml乙二胺四醋酸二钠滴定液(0.01mol/L)相当于2.7723mg的C10H24N2O2•2HCl。
抗结核病药。
遮光,密封保存。
杂质Ⅰ
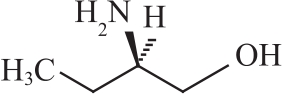
(+)2-氨基丁醇
杂质Ⅱ(内消旋-乙胺丁醇)
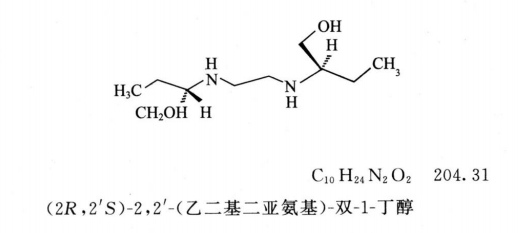
杂质Ⅲ[(R,R)-乙胺丁醇]
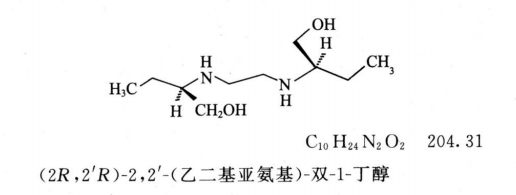
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
