登录/
注册
登录/
注册
卡托普利
Katuopuli
Captopril
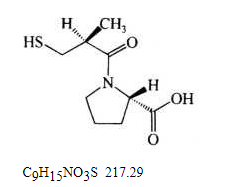
本品为1-[(2S)-2-甲基-3-巯基-丙酰基]-L-脯氨酸。按干燥品计算,含C9H15NO3S不得少于97.5%。
本品为白色或类白色结晶性粉末;有类似蒜的特臭。
本品在甲醇、乙醇或三氯甲烷中易溶,在水中溶解。
熔点 本品的熔点(通则0612)为104~110℃。
比旋度 取本品,精密称定,加乙醇溶解并定量稀释制成每1ml中约含20mg的溶液,依法测定(通则0621),比旋度为-126°至-132°。
①高血压,可单独应用或与其他降压药如利尿药合用;②心力衰竭,可单独应用或与强心药利尿药合用;③高血压急症(注射药)。④诊断肾血管性高血压试验用药。
成人 ①降压,口服一次 12.5mg,一日2~3次,按需要1~2周增至一次25mg,一日 2~3次;疗效不满意时可加用利尿药。②治疗心力衰竭,开始一次口服 12.5mg,一日 2~3次,必要时逐渐递增至一次 25~50mg,一日 2~3 次;若需进一步加量,宜观察疗效2周后再考虑。
用于肾血管性高血压药物诊断;在常规肾图或肾动态检查后当日,口服卡托普利 25 ~50 mg(粉末状),每隔15分钟测一次血压至 60分钟,饮水300~500ml 或 8ml/kg后进行常规肾图或肾动态显像。
【儿科用法与用量】口服 一日开始1mg/kg,逐渐增加,求得最低有效量,最大可增至一日6mg/kg,分3次服。
【儿科注意事项】 皮疹、头痛、眩晕、血管性水肿、蛋白尿、白细胞与粒细胞减少等。
(1)药效学
①降压,本品为竞争性血管紧张素转换酶抑制药,使血管紧张素Ⅰ不能转化为血管紧张素Ⅱ,结果血浆肾素活性增高,醛固酮分泌减少,血管阻力减低。本品还抑制缓激肽的降解;也可直接作用于周围血管而降低阻力,心排血量不变或增多,肾小球滤过率不变。卧位与立位降压作用无差别。②减低心脏负荷,心力衰竭时本品扩张动脉与静脉,降低周围血管阻力或后负荷,减低肺毛细血管嵌顿压或前负荷,也降低肺血管阻力,因而改善心排血量,运动耐量时间延长。
(2)药动学
口服本品后吸收迅速,吸收率在75%以上,餐中服用胃肠道内有食物存在可使本品的吸收减少30%~40%,故宜在餐前1小时服药。血循环中本品的25%~30%与蛋白结合。用于降压,口服后15分钟开始起效,1~1.5小时作用达高峰,持续6~12小时,其时间长短与剂量相关。降压作用进行性,约数周达最大治疗作用,t1/2β小于3小时,肾功能衰竭时延长。在肝内代谢为二硫化物等。经肾排泄,约40%~50%以原形排出,其余为代谢物,可在血液透析时被清除。本品不能通过血-脑屏障。注射本品 15 分钟后生效,1~2小时作用达高峰,持续4~6小时。
(1)较常见 ①皮疹,可能伴有瘙痒和发热,7%~10%伴嗜酸粒细胞增多,或抗核抗体阳性;②心悸、心动过速、胸痛;③咳嗽;④味觉迟钝。
(2)较少见 眩晕、头痛、昏厥。由低血压引起,尤其在缺钠或血容量不足及血管性水肿时发生,见于面部及手脚,也可引起舌、声门或喉血管性水肿;面部潮红或苍白。
(3)极少见 白细胞与粒细胞减少,有发热、寒战,白细胞减少与药量相关,治疗开始后3~12 周出现,以10~30天最显著,停药后持续2周。逾量可致低血压,应立即停药,并扩容以纠正,在成人还可用血液透析清除。
(1)对本品或其他血管紧张素转换酶抑制药过敏者。
(2)孤立肾、移植肾、双侧肾动脉狭窄、严重肾功能减退者。
(3)妊娠、哺乳期妇女。
(4)美国FDA妊娠期药物安全性分级为口服给药C;如在妊娠中、晚期用药为D。
(1)曾有报告本品在婴儿可引起血压过度与持久降低伴少尿与抽搐,故应用本品仅限于其他降压治疗无效者。
(2)老年人对降压作用较敏感,应用本品须酌减剂量。特别是首次服用。
(3)对诊断的干扰 用本品时可有①血尿素氮、肌酐浓度增高,常为暂时性,在有肾病或长期严重高血压而血压迅速下降后易出现;②偶有血清肝脏酶增高;③血钾轻度增高,尤其有肾功能障碍者,与保钾利尿药合用时尤注意检查血钾;④血钠减低。
(4)下列情况慎用本品 ①自身免疫性疾病如严重系统性红斑狼疮,此时白细胞或粒细胞减少的机会增多;②骨髓抑制;③脑动脉或冠状动脉供血不足,可因血压降低而缺血加剧;④血钾过高;⑤肾功能障碍而致血钾增高、白细胞及粒细胞减少,并使本品潴留;⑥主动脉瓣狭窄,此时可能使冠状动脉灌注减少;⑦严格饮食限制钠盐或进行透析者,此时首剂应用本品可能发生突然而严重的低血压。
(5)在手术或麻醉时用本品发生低血压,可用扩容纠正。
(6)用本品时若白细胞计数过低,暂停用本品可以恢复。
(7)用本品治疗心力衰竭,无液体潴留,并使血醛固酮水平降低,为其优点,但须注意降压反应。
(8)用本品时出现血管神经性水肿,应停用本品,迅速皮下注射1∶1000肾上腺素0.3~0.5ml。
(9)用本品期间随访检查∶①白细胞计数及分类计数,最初3个月内每2周一次,此后定期检查,有感染迹象时随即检查;②尿蛋白检查,每月1次。
(1)与利尿药同用使降压作用增强,但应避免引起严重低血压,故原用利尿药者宜停药或减量,本品开始用小剂量,逐渐调整剂量。
(2) 与其他扩血管药同用可能致低血压,如拟合用,应从小剂量开始。
(3)与潴钾药物如螺内酯、氨苯蝶啶、阿米洛利同用可能引起血钾过高。
(4)与内源性前列腺素合成抑制药如吲哚美辛同用,将使本品降压作用减弱。
(5)与其他降压药合用,降压作用加强,与引起肾素释出或影响交感活性的药物呈相加作用,与β受体拮抗药呈小于相加的作用。
卡托普利片∶ (1)12.5mg;(2)25mg;(3)50mg。
(1)取本品约25mg,加乙醇2ml溶解后,加亚硝酸钠结晶少许与稀硫酸10滴,振摇,溶液显红色。
(2) 取卡托普利二硫化物项下的供试品溶液,用流动相稀释制成每1ml中含0.1mg的溶液,作为供试品溶液;另取卡托普利对照品,加甲醇适量溶解,再用流动相稀释制成每1ml中约含0.1mg的溶液,作为对照品溶液。照卡托普利二硫化物项下的色谱条件,取供试品溶液与对照品溶液各20μl,分别注入液相色谱仪,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(3) 本品的红外光吸收图谱应与对照的图谱(光谱集96图)一致。
卡托普利二硫化物(杂质Ⅰ) 照高效液相色谱法(通则0512)测定。避光操作。
供试品溶液 临用新制。取本品,精密称定,加流动相溶解并定量稀释制成每1ml中约含0.5mg的溶液。
对照品溶液 取杂质Ⅰ对照品,精密称定,加甲醇适量溶解,再用流动相定量稀释制成每1ml中约含5μg的溶液。
系统适用性溶液 取卡托普利与杂质Ⅰ对照品,加甲醇适量溶解,用流动相稀释制成每1ml中各约含0.1mg与15μg的混合溶液。
色谱条件 以十八烷基硅烷键合硅胶为填充剂;0.01mol/L磷酸二氢钠溶液-甲醇-乙腈(70:25:5)(用磷酸调节pH值至3.0)为流动相;检测波长为215nm;柱温40℃;进样体积50μl。
系统适用性要求 系统适用性溶液色谱图中,卡托普利峰与杂质Ⅰ峰之间的分离度应大于4.0。
测定法 精密量取供试品溶液与对照品溶液,分别注入液相色谱仪,记录色谱图。
限度 供试品溶液色谱图中如有与杂质Ⅰ峰保留时间一致的色谱峰,按外标法以峰面积计算,不得过1.0%。
硫酸盐 取本品1.0g,依法检查(通则0802),与标准硫酸钾溶液5.0ml制成的对照液比较,不得更浓(0.05%)。
干燥失重 取本品,以五氧化二磷为干燥剂,在60℃减压干燥至恒重,减失重量不得过0.5%(通则0831)。
炽灼残渣 取本品2.0g,依法检查(通则0841),遗留残渣不得过0.1%。
重金属 取炽灼残渣项下遗留的残渣,加硝酸1ml,蒸干至氧化氮蒸气除尽,加盐酸2ml,置水浴上蒸干,再加水5ml,蒸干,加水15ml与醋酸盐缓冲液(pH 3.5)4ml,微温使溶解,加水使成50ml,摇匀,分取25ml,依法检查(通则0821第一法),含重金属不得过百万分之二十。
锌盐 取上述重金属项下剩余的溶液25ml,置50ml纳氏比色管中,加盐酸溶液(1→2)4ml与亚铁氰化钾试液3ml,加水至刻度,摇匀,如发生浑浊,与标准锌溶液[精密称取硫酸锌(ZnSO4·7H2O)44mg,置100ml量瓶中,加水溶解并稀释至刻度,摇匀,精密量取10ml,置另一100ml量瓶中,加水稀释至刻度,摇匀。每1ml相当于10μg的Zn]3.0ml制成的对照液比较,不得更浓(0.003%)。
取本品约0.3g,精密称定,加水100ml,振摇使溶解,加稀硫酸10ml,再加碘化钾1.0g与淀粉指示液2ml,用碘酸钾滴定液(0.016 67mol/L)滴定,至溶液显微蓝色(保持30秒不褪色),并将滴定的结果用空白试验校正。每1ml碘酸钾滴定液(0.016 67mol/L)相当于21.73mg的C9H15NO3S。
遮光,密封保存。
杂质Ⅰ(卡托普利二硫化物)
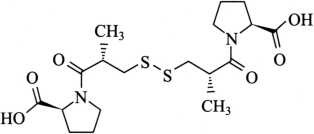
C18H28N2O6S2 432.55
(2S,2'S)-1,1'-[二硫烷二基双[(2S)-2-甲基-1-氧代丙烷-3,1-二基]-双[吡咯烷-2-羧酸]]
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
