登录/
注册
登录/
注册
美司钠
Meisina
Mesna
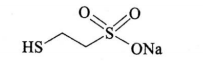
C2H5NaO3S2 164.18
本品为2-巯乙磺酸钠。按干燥品计算,含C2H5NaO3S2应为96.0%~102.0%。
本品为白色或类白色粉末或结晶性粉末;有引湿性。
本品在水中易溶,在甲醇中略溶,在乙醇中微溶,在丙酮、三氯甲烷或乙醚中不溶。
用于接受环磷酰胺或异环磷酰胺治疗的患者,作为泌尿系统保护药,预防上述药物的代谢产物所致以出血性膀胱炎等为主的泌尿道毒性。
静脉注射常用量为异环磷酰胺或环磷酰胺的20%,例如异环磷酰胺一次2000mg,则本品一次400mg,注射时间分别于异环磷酰胺给药后的0小时(即应用抗肿瘤制剂的同一时间)、4小时和8小时。
(1)药效学 环磷酰胺类化疗药在体内产生的丙烯醛和4-羟基代谢物对泌尿道有一定的毒性。本品可与丙烯醛的双链结合,形成稳定的硫醚化合物;另外,本品可减低尿中4-羟基代谢产物的降解速度,形成一种相对稳定的4-羟基环磷酰胺或4-羟基异环磷酰胺与美司钠缩合而成的物质,此物质对膀胱无毒性。
(2)药动学 本品静脉注射后主要分布于肾脏,并可迅速在组织中转化为无生物活性的二硫化物,经肾小球滤过后,在肾小管上皮又转变成巯乙磺酸钠。本品吸收后立即开始代谢,并于8小时内大部分清除。人体血浆半衰期约为1.5小时。24小时内约有80%的药物从尿中排泄。
(1)常规剂量给药,一般无不良反应,若大剂量按体重每次超过60~70mg/kg时,可能出现恶心、呕吐、腹痛和腹泻等。
(2)极少数可出现静脉刺激和皮肤或黏膜过敏反应。
对含巯基化合物过敏者禁用。
(1)本品的保护作用只限于泌尿系统的损害。
(2)当使用本品治疗时可引起尿酮试验假阳性反应。
(3)妊娠期妇女及哺乳期妇女慎用。
(4)易于呕吐或恶心以及胃肠道吸收障碍患者,不宜口服本品。
本品与华法林合用,出血的危险性增加。本品与顺铂和氮芥不能配伍。
美司钠注射液:(1)2ml:200mg;(2)4ml:400mg。
(1)取本品约10mg,加水2ml溶解后,加亚硝酸钠少许和稀硫酸10滴,振摇,溶液显红色。
(2)本品的红外光吸收图谱应与对照的图谱(光谱集1174)—致。
(3)本品显钠盐的鉴别反应(通则0301)。
酸度 取本品1.0g,加水10ml使溶解,依法测定(通则0631),pH值应为4.0~6.0。
溶液的澄清度与颜色 取本品1.0g,加水10ml溶解后,溶液应澄清无色。
氯化物 取本品0.2g,依法检查(通则0801),与标准氯化钠溶液5.0ml制成的对照液比较,不得更浓(0.025%)。
硫酸盐 取本品1.0g,依法检查(通则0802),与标准硫酸钾溶液3.0ml制成的对照液比较,不得更浓(0.03%)。
有关物质照高效液相色谱法(通则0512)测定。
供试品溶液 取本品适量,精密称定,加流动相溶解并定量稀释制成每1ml中约含4mg的溶液。
对照溶液 精密量取供试品溶液适量,用流动相定量稀释制成每1ml中约含0.012mg的溶液。
对照品溶液 取杂质I(双硫化合物)对照品适量,精密称定,加流动相溶解并定量稀释制成每1ml中约含0.12mg的溶液。
系统适用性溶液 取供试品溶液与对照品溶液各适量,加流动相稀释制成每1ml中含美司钠和杂质I分别约为0.18mg和0.005mg的混合溶液。
灵敏度溶液 精密量取对照溶液适量,用流动相定量稀释制成每1ml中约含0.8μg的溶液。
色谱条件 用十八烷基硅烷键合硅胶为填充剂(GeminiCl8色谱柱,4.6mm×250mm,5μm或效能相当的色谱柱);以甲醇-磷酸盐缓冲液(取磷酸二氢钾2.94g、磷酸氢二钾2.94g、四丁基硫酸氢铵2.6g溶于660ml水中,用磷酸调pH值为2.3)(34∶66)为流动相;检测波长为235nm;进样体积20μl。
系统适用性 要求系统适用性溶液色谱图中,美司钠峰与杂质I峰的分离度应大于5.0;灵敏度溶液色谱图中,美司钠峰高的信噪比应大于10。
测定法 精密量取供试品溶液、对照品溶液与对照溶液,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的4倍。
限度 供试品溶液色谱图中如有与杂质I峰保留时间一致的色谱峰,按外标法以峰面积计算,含杂质I不得过3.0%;与美司钠峰(保留时间约为4.8分钟)比较,相对保留时间约为0.6(可能包含杂质II、杂质III或杂质IV,按总和计)及0.8(杂质V)的杂质峰,按校正后的峰面积计算(均乘以校正因子0.01),均不得大于对照溶液主峰面积(0.3%);其他单个未知杂质峰面积不得大于对照溶液主峰面积的1/3(0.1%),其他单个未知杂质峰面积的和不得大于对照溶液主峰面积(0.3%)。供试品溶液色谱图中小于灵敏度溶液主峰面积的色谱峰忽略不计(0.02%)。
残留溶剂照残留溶剂测定法(通则0861)测定,应符合规定。
干燥失重 取本品,在60℃减压干燥2小时,减失重量不得过1.0%(通则0831)。
重金属 取本品1.0g,依法检查(通则0821第三法),含重金属不得过百万分之十。
取本品约0.12g,精密称定,加水10ml,振摇使溶解,加稀硫酸10ml,精密加入碘滴定液(0.05mol/L)10ml,摇匀,用硫代硫酸钠滴定液(0.1mol/L)滴定,至近终点时,加淀粉指示液1ml,继续滴定至蓝色消失,并将滴定的结果用空白试验校正。每1ml硫代硫酸钠滴定液(0.1mol/L)相当于16.42mgC2H5NaO3S2。
抗肿瘤辅助药。
遮光,密封保存。
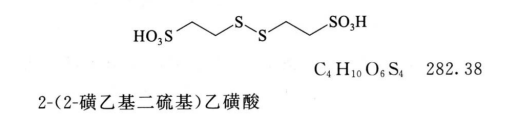
杂质Ⅰ(双硫化合物)
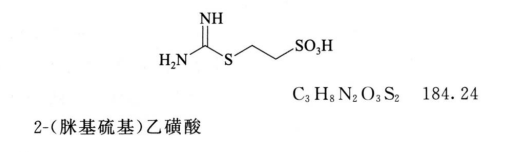
杂质Ⅱ
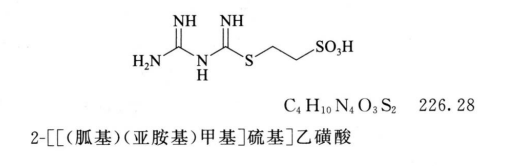
杂质Ⅲ
杂质Ⅳ
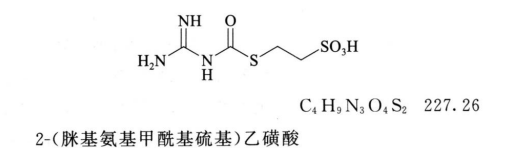
杂质V
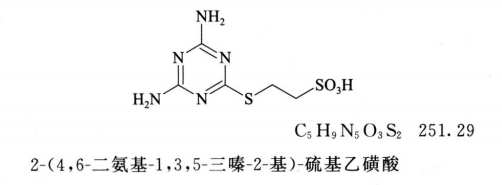
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
