登录/
注册
登录/
注册
盐酸米托蒽醌
YansuanMituoenkun
MitoxantroneHydrochloride
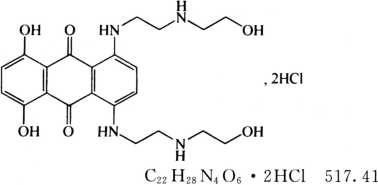
本品为1,4-二羟基-5,8-双[[2-[(2-羟乙基)氨基]乙基]氨基-9,10-蔥醌二盐酸盐。按无水物计算,含C22H28N4O6·2HCl应为97.0%~102.0%。
本品为蓝黑色结晶性粉末;无臭;有引湿性。
本品在水中溶解,在乙醇中微溶,在三氯甲烷中不溶。
本品主要用于恶性淋巴瘤、乳腺癌和急性白血病。对肺癌、黑色素瘤、软组织肉瘤、多发性骨髓瘤、肝癌、大肠癌、肾癌、前列腺癌、子宫内膜癌、睾丸肿瘤、卵巢癌和头颈部癌也有一定疗效。
静脉滴注(1)单药治疗成人按体表面积一次10mg/m²,溶于5%葡萄糖注射液100ml内,静脉滴注30分钟,每3~4周1次。
(2)联合用药成人按体表面积一次6~8mg/m²。其他同单药治疗。
(1)药效学 作用机制尚不清楚,可能抑制脱氧核糖核酸(DNA)及核糖核酸(RNA)合成。有报道在体外实验中可抑制H-胸腺嘧啶核苷掺入DNA和H-尿嘧啶核苷掺入RNA的能力。本品与DNA有两种结合形式:一是与碱基强有力结合而嵌入DNA,引起DNA链间和链内交叉连接,导致DNA单链及双链断裂;另一较弱的结合是通过与螺旋链外部阴离子的静电作用,此外对RNA聚合酶也有抑制作用。本品对各细胞周期肿瘤细胞均有抑制作用,但主要作用于S后期。
(2)药动学 本品静脉滴注后,血药浓度下降很快,并迅速分布于各组织中,消除缓慢。本品分布容积为522L/m²,血浆蛋白结合率为78%。半衰期为40~120小时,有腹水者半衰期可进一步延长。本品主要在肝脏代谢,分解为一羧基酸与二羧基酸。代谢物主要由粪便排出,6%~11%经肾脏排泄(其中65%为原形药),可分泌入乳汁。
(1)骨髓抑制主要是白细胞及血小板减少。
(2)胃肠道反应食欲缺乏、恶心、呕吐等。
(3)心脏毒性本品还原力强,不易形成氧自由基及脂质体超氧化,故心脏毒性较多柔比星轻,主要表现为心肌肥大和纤维化。心脏毒性发生率与本品总剂量有关,总剂量超过140~160mg/m²,心肌损害增加;在用过多柔比星、纵隔部位接受过放射治疗或原有心脏疾病的患者,总剂量不宜超过100~120mg/m²。本品发生心力衰竭的最低剂量为55~255mg/m²,发生左心室排血量减少的最低剂量为21~150mg/m²。在多柔比星总剂量超过450mg/m²的患者不宜再用本品,在总剂量超过350mg/m²的患者,也应在严密观察下使用本品。
(4)偶见乏力、脱发、皮疹、口腔炎等。
(1)对本品有过敏史者禁用。
(2)妊娠期妇女及哺乳期妇女禁用。
(1)用药过程中,应注意有无咳嗽、气急、水肿等提示心力衰竭的症状。应密切随访周围血象,肝、肾功能,心电图,必要时还需测定左心室排血量、超声心动图等。
(2)不宜做鞘内注射,可能会引起截瘫。
(3)本品由尿排出,可使尿呈蓝色,不需处理。
(1)与多柔比星同用可加重心脏毒性。
(2)本品有骨髓抑制作用,与其他抗肿瘤药物联合应用时应注意。
盐酸米托蒽醌注射液:(1)2ml:2mg;(2)5ml:5mg;(3)10ml:10mg。
注射用盐酸米托蒽醌:(1)2mg;(2)5mg;(3)10mg;(4)20mg;(5)25mg。
(1)取本品约5mg,加水1ml溶解后,加浓硫酸1ml,溶液由深蓝色变为深紫红色。
(2)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(3)本品的红外光吸收图谱应与对照的图谱(光谱集824图)一致。
(4)本品显氯化物的鉴别反应(通则0301)。
酸度 取本品0.10g,加水10ml溶解后,依法测定(通则0631),pH值应为3.0~5.5。
有关物质照高效液相色谱法(通则0512)测定。
供试品溶液 取本品,加流动相溶解并稀释制成每1ml中约含1mg的溶液。
对照溶液 精密量取供试品溶液1ml,置100ml量瓶中,用流动相稀释至刻度,摇匀。
系统适用性溶液 取盐酸米托蔥醌约2.5mg,加流动相5ml溶解,精密加1.0mol/L氢氧化钠溶液1ml,立即置90℃水浴中准确加热4分钟,取出迅速放冷,精密加1.0mol/L盐酸溶液1ml,混匀。
色谱条件 用十八烷基硅烷键合硅胶为填充剂;以庚烷磺酸钠溶液(取庚烷磺酸钠4.4g,加水适量使溶解,加冰醋酸6.4ml,用水稀释至730ml)-乙腈(70∶30)为流动相;检测波长为244nm;进样体积20μl。
系统适用性 要求理论板数按米托蔥醌峰计算不低于2000。系统适用性溶液色谱图中,米托蔥醌主峰与其后的最大降解峰之间的分离度应大于5.0。
测定法 精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的2倍。
限度 供试品溶液色谱图中如有杂质峰,单个杂质峰面积不得大于对照溶液主峰面积(1.0%),各杂质峰面积的和不得大于对照溶液主峰面积的2倍(2.0%)。
水分 取本品,照水分测定法(通则0832第一法1)测定,含水分不得过5.0%。
炽灼残渣 取本品1.0g,依法检查(通则0841),遗留残渣不得过0.2%。
重金属 取炽灼残渣项下遗留的残渣,依法检查(通则0821第二法),含重金属不得过百万分之二十。
照高效液相色谱法(通则0512)测定。
供试品溶液 取本品适量,精密称定,加水溶解并定量稀释制成每1ml中约含0.1mg的溶液。
对照品溶液 取盐酸米托蔥醌对照品适量,精密称定,加水溶解并定量稀释制成每1ml中约含0.1mg的溶液。
系统适用性溶液、色谱条件与系统适用性要求见有关物质项下。
测定法 精密量取供试品溶液与对照品溶液,分别注入液相色谱仪,记录色谱图。按外标法以峰面积计算。
抗肿瘤药。
遮光,密封保存。
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
