登录/
注册
登录/
注册
盐酸西替利嗪
YansuanXitiliqin
CetirizineHydrochloride
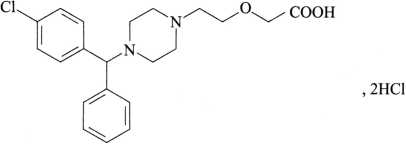
C21H25ClN2O3·2HCl 461.81
本品为(±)-2-[2-[4-[(4-氯苯基)苯甲基]-1-哌嗪基]乙氧基]乙酸二盐酸盐。按干燥品计算,含C21H25ClN2O3·2HCl不得少于99.0%。
本品为白色或类白色结晶性粉末,无臭。
本品在水中易溶,在甲醇或乙醇中溶解,在三氯甲烷或丙酮中几乎不溶。
吸收系数 取本品约20mg,精密称定,置100ml量瓶中,加0.1mol/L盐酸溶液使溶解并稀释至刻度,摇匀;精密量取5ml,置100ml量瓶中,用0.1mol/L盐酸溶液稀释至刻度,摇匀,照紫外-可见分光光度法(通则0401),在231nm的波长处测定吸光度,吸收系数(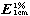 )为365~385。
)为365~385。
①用于过敏性鼻炎、过敏性结膜炎;②荨麻疹;③各种过敏性瘙痒性皮肤疾患。
口服一次10mg,一日1次,或一次5mg,一日2次。
【儿科用法与用量】口服2~6岁,一日5mg,分1~2次;6~12岁,一日10mg,分1~2次。
外用1~2岁可用滴剂,一次2.5mg,一日1~2次。
【儿科注意事项】偶见嗜睡等镇静作用。
(1)药效学 本品为羟嗪的衍生物,可选择性拮抗H₁受体,可抑制由组胺介导的过敏反应的初始期,同时还可明显减少与迟发性皮肤过敏反应相关的炎性细胞(如嗜酸粒细胞)的迁移及炎性介质的释放。本品不易通过血-脑屏障,有一定抗胆碱作用。
(2)药动学 口服本品在5~60mg剂量范围内,血浆浓度水平与给药剂量呈线形关系。成年人清除相半衰期(t1/2β)约为10小时,给药剂量的2/3以原形由尿液排出。本品的吸收不受进食的影响。
①偶见嗜睡、头晕、头痛、激动、口干、胃肠不适;②罕见过敏反应报道。
(1)对本品及辅料过敏者禁用。
(2)对羟嗪过敏者也应禁用。
(1)驾驶及操作精密或危险机械者慎用。
(2)肾功能不全者慎用。
(3)美国FDA妊娠期药物安全性分级为口服给药B。
同服镇静剂(安眠药)及乙醇时需小心。
盐酸西替利嗪片:10mg。
盐酸西替利嗪滴剂:(1)5ml:50mg;(2)10ml:100mg。
盐酸西替利嗪糖浆:0.1%(g/ml)。
盐酸西替利嗪口服溶液:10ml:10mg。
盐酸西替利嗪胶囊:(1)5mg;(2)10mg。
(1)照薄层色谱法(通则0502)试验。
供试品溶液 取本品约10mg,加甲醇适量,振摇使溶解,用甲醇稀释至100ml,摇匀。
对照品溶液 取盐酸西替利嗪对照品适量,加甲醇溶解并稀释制成每1ml中约含0.1mg的溶液。
色谱条件采用硅胶G薄层板,以二氯甲烷-甲醇-浓氨溶液(4∶1∶0.2)为展开剂。
测定法 吸取供试品溶液与对照品溶液各10μl,分别点于同一薄层板上,展开,晾干,置碘蒸气中显色后,立即检视。
结果判定供试品溶液所显主斑点的颜色和位置应与对照品溶液的主斑点一致。
(2)取本品适量,加0.1mol/L盐酸溶液溶解并稀释制成每1ml中约含10μg的溶液,照紫外-可见分光光度法(通则0401)测定,在231nm的波长处有最大吸收,在218nm的波长处有最小吸收。
(3)本品的红外光吸收图谱应与对照的图谱(光谱集826图)一致。
(4)本品的水溶液应显氯化物鉴别(1)的反应(通则0301)。
酸度 取本品0.50g,加水10ml使溶解后,依法测定(通则0631),pH值应为1.2~1.8。
溶液的澄清度与颜色 取本品1.0g,加水10ml使溶解,溶液应澄清无色;如显色,与黄绿色1号标准比色液(通则0901第一法)比较,不得更深。
氰化物 取本品1.0g,依法检查(通则0806第一法),应符合规定。
有关物质照高效液相色谱法(通则0512)测定。
供试品溶液 取本品适量,加水使溶解并稀释制成每1ml中约含0.2mg的溶液。
对照溶液 精密量取供试品溶液适量,用水定量稀释制成每1ml中约含2μg的溶液。
灵敏度溶液 精密量取对照溶液适量,用水定量稀释制成每1ml中约含0.2μg的溶液。
色谱条件 用十八烷基硅烷键合硅胶为填充剂;以乙腈-0.1%三乙胺的0.05mol/L磷酸二氢钠溶液(用磷酸调节pH值至3.0)(35∶65)为流动相;检测波长为230nm;进样体积20μl。
系统适用性 要求理论板数按西替利嗪峰计算不低于4000。灵敏度溶液色谱图中,主成分峰高的信噪比应不小于10。
测定法 精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的3倍。
限度供试品溶液色谱图中如有杂质峰,单个杂质峰面积不得大于对照溶液主峰面积的0.5倍(0.5%),各杂质峰面积的和不得大于对照溶液主峰面积(1.0%)。
干燥失重 取本品,在105℃干燥至恒重,减失重量不得过0.5%(通则0831)o
炽灼残渣 取本品1.0g,依法检查(通则0841),遗留残渣不得过0.1%。
重金属 取炽灼残渣项下遗留的残渣,依法检查(通则0821第二法),含重金属不得过百万分之十。
取本品约0.18g,精密称定,加冰醋酸20ml溶解后,加醋酸汞试液5ml与结晶紫指示液1滴,用高氯酸滴定液(0.1mol/L)滴定至溶液显蓝色,并将滴定的结果用空白试验校正。每1ml高氯酸滴定液(0.1mol/L)相当于23.09mg的C21H25ClN2O3·2HCl。
组胺H1受体拮抗剂。
密封保存。
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
