登录/
注册
登录/
注册
盐酸氮䓬斯汀
Yansuan Danzhuositing
Azelastine Hydrochloride
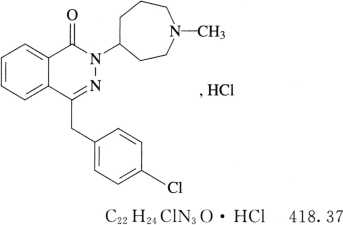
本品为(±)4-(4-氯苄基)-2-(六氢-1-甲基-1H-氮杂䓬-4-基)-l(2H)-2,3-二氮杂萘酮盐酸盐。按干燥品计算,含C22H24ClN3O·HCl不得少于99.0%。
本品为白色或类白色粉末或结晶性粉末;无臭。
本品在甲醇中略溶,在水或乙醇中微溶,在冰醋酸中溶解。
①预防和治疗季节性过敏性鼻结膜炎;②慢性特发性荨麻疹;③常年性过敏性鼻炎;④用于哮喘的辅助治疗。
口服片剂①成人一次1~4mg,一日2次。②6~12岁儿童一次2mg,一日2次。
外用(1)喷鼻剂成人及6岁以上儿童一次每鼻孔1喷,一日2次,或遵医嘱,可用至症状消除,但不能连续使用超过6个月。
(2)滴眼剂一次1滴滴眼,一日2~4次。
(1)药效学 本品为H1受体拮抗药,并能稳定肥大细胞膜从而抑制炎性介质从肥大细胞释放,拮抗多种炎性介质如白三烯、血小板活化因子等,还可抑制嗜酸粒细胞的浸润,从多渠道发挥抗组胺作用。
(2)药动学 口服后,吸收迅速完全,4~5小时达血药浓度峰值。经肝脏代谢,其主要代谢产物为去甲基氮䓬斯汀,后者仍具抗组胺活性。氮䓬斯汀及其代谢产物的血浆清除半衰期(t1/2β)约为25小时,其血浆蛋白结合率分别为88%和97%。氮䓬斯汀及其代谢产物主要从粪便排出,在尿中亦有排泄。口服给药后,药代动力学参数不受年龄、性别或肝功能损害的影响。
(1)口服本品可有困倦、口干、鼻干、口苦,偶见便秘、头痛、ALT升高。
(2)滴眼剂可有轻微、短暂的局部刺激感、苦味等。
(3)喷鼻剂可有鼻黏膜刺激感、鼻出血等一过性反应。
(1)对本品及辅料过敏者禁用。
(2)美国FDA妊娠期药物安全性分级为眼部给药C。
(1)服药期间不要驾驶车辆、操作机器及进行高空作业。
(2)本品应避免与乙醇或其他中枢抑制药物同时服用。
(3)哺乳期妇女不推荐服用本品。
(4)低龄儿童及老人不推荐服用本品。
(5)应用本品滴眼剂期间不能配戴角膜接触镜。
西咪替丁可增加口服本品峰浓度(Cmax)和曲线下面积(AUC)约65%;酮康唑干扰本品血药浓度的测定,但对Q-T间期无影响;口服雷尼替丁、红霉素、氨茶碱对本品药代动力学无明显影响。
盐酸氮䓬斯汀片:(1)1mg;(2)2mg。
盐酸氮䓬斯汀鼻喷雾剂:(1)10ml:10mg。70喷,每喷0.14mg;(2)10ml:10mg;140喷,每喷0.07mg。
盐酸氮䓬斯汀滴眼液:(1)5ml:2.5mg;(2)8ml;4mg(0.05%);(3)6ml:3mg。
(1)取本品适量,加水溶解并稀释制成每1ml中约含30μg的溶液,照紫外-可见分光光度法(通则0401)测定,在286nm的波长处有最大吸收,在264nm的波长处有最小吸收。
(2)本品的红外光吸收图谱应与对照品的图谱一致(通则0402)。
(3)本品的水溶液显氯化物鉴别(1)的反应(通则0301)。
旋光度 取本品适量,精密称定,加水溶解并定量稀释制成每1ml中约含5mg的溶液(必要时可超声助溶),依法测定(通则0621),旋光度为-0.01°至+0.01°。
酸度 取本品50mg,加水30ml使溶解(必要时可超声助溶),依法测定(通则0631),pH值应为5.0~7.0。
有关物质 照高效液相色谱法(通则0512)测定。
供试品溶液 取本品适量,加流动相溶解并稀释制成每1ml中约含1mg的溶液。
对照溶液 精密量取供试品溶液1ml,置200ml量瓶中,用流动相稀释至刻度,摇匀。
色谱条件 用十八烷基硅烷键合硅胶为填充剂;以4%三乙胺溶液(用磷酸调节pH值至6.0)-乙腈-甲醇(50∶18∶32)为流动相;检测波长为289nm;进样体积20μl。
系统适用性要求 理论板数按氮䓬斯汀峰计算不低于3000,氮䓬斯汀峰与相邻杂质峰之间的分离度应符合要求。
测定法 精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的2倍。
限度 供试品溶液色谱图中如有杂质峰,单个杂质峰面积不得大于对照溶液主峰面积的0.4倍(0.2%),各杂质峰面积的和不得大于对照溶液主峰面积(0.5%)。
残留溶剂 照残留溶剂测定法(通则0861第二法)测定。
内标溶液 取乙酸乙酯适量,加50%N,N-二甲基甲酰胺溶液制成每1ml中约含乙酸乙酯80μg的溶液。
供试品溶液 取本品约0.1g,精密称定,置顶空瓶中,精密加入5ml内标溶液使溶解,密封。
对照品溶液 精密称取甲醇、乙醇、异丙醇、丙酮与二氯甲烷各适量,加内标溶液溶解并定量稀释制成每1ml中约含甲醇60μg、乙醇100μg、丙酮100μg、异丙醇100μg与二氯甲烷12μg的混合溶液,精密量取5ml,置顶空瓶中,密封。
色谱条件 以6%氰丙基苯基-94%二甲基聚硅氧烷(或极性相近)为固定液的毛细管柱为色谱柱;起始温度为40℃,维持8分钟,以每分钟60℃速率升温至160℃,维持2分钟;检测器温度为250℃;进样口温度为200℃;顶空瓶平衡温度为85℃,平衡时间为15分钟。
系统适用性要求 对照品溶液色谱图中,各成分峰之间的分离度均应符合要求。
测定法 取供试品溶液与对照品溶液,分别顶空进样,记录色谱图。
限度 按内标法以峰面积计算,甲醇、乙醇、异丙醇、丙酮与二氯甲烷的残留量均应符合规定。
干燥失重 取本品,在105℃干燥至恒重,减失重量不得过1.0%(通则0831)。
炽灼残渣 取本品1.0g,依法检查(通则0841),遗留残渣不得过0.1%。
重金属 取炽灼残渣项下遗留的残渣,依法检查(通则0821第二法),含重金属不得过百万分之二十。
取本品约0.3g,精密称定,加无水甲酸5ml与醋酐30ml溶解后,照电位滴定法(通则0701),用高氯酸滴定液(0.1mol/L)滴定,并将滴定的结果用空白试验校正。每1ml高氯酸滴定液(0.1mol/L)相当于41.84mg的C22H24ClN3O·HCl。
H1受体拮抗剂。
密封保存。
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
