登录/
注册
登录/
注册
盐酸多奈哌齐
YansuanDuonaipaiqi
DonepezilHydrochloride
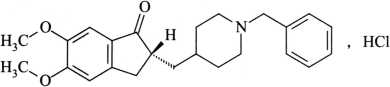
C24H29NO3·HCl 415.95
本品为(±)-2-[(1-苄基-4-哌啶基)甲基]-5,6-二甲氧基-1-茚酮盐酸盐。按干燥品计算,含C24H29NO3·HCl应为98.0%~102.0%。
本品为白色或类白色结晶性粉末。
本品在三氯甲烷中易溶,在水中溶解,在乙醇中略溶;在盐酸溶液(1→1000)中略溶。
①轻至中度认知障碍的阿尔茨海默病;②血管性痴呆。
口服一次5~10mg,一日1次。
(1)药效学 本品通过抑制胆碱酯酶活性,提高脑内乙酰胆碱的含量,改善阿尔茨海默病患者的记忆障碍和认知功能。
(2)药动学 口服吸收良好,达峰时间(tmax)为3~4小时。每日口服1~10mg,血浓度与剂量呈线性相关。食物和服药时间均不影响药物的吸收。半衰期(t1/2)约70小时,多次服药3周后达稳态浓度(Css)。表观分布容积(Vd)为12L/kg。血浆蛋白结合率96%,其中75%与白蛋白结合,21%与α酸性糖蛋白结合。部分药物在肝脏经CYP3A4和CYP2D6代谢,生成4种主要代谢产物,口服量的11%生成6-O-去甲多奈哌齐,其生物活性与母体相似。服药10日后,57%以原形药物和代谢产物从尿中排出,15%从粪便排出,但有28%未见排出,提示体内有蓄积。此后可发现约17%以原形药物从尿中排出。
(1)主要不良反应恶心、呕吐、食欲缺乏、胃部不适、腹胀、腹泻、眩晕、高血压或低血压等;谵妄、震颤、易激惹、共济失调、情感不稳、神经痛、肌肉痉挛、肌张力过低、动作减少、抽搐、妄想、失眠等;胸痛、鼻塞、流涕、尿频、尿急、血尿;肌酸磷酸激酶、乳酸脱氢酶和血糖升高,体重增加;眼部刺痛、眼干、耳鸣、听力减退、疲劳等。
(2)严重不良反应房室传导阻滞、心房颤动、尖端扭转型室性心动过速、心绞痛、充血性心力衰竭等。
(1)对多奈哌齐或六氢吡啶类衍生物过敏者。
(2)美国FDA妊娠期药物安全性分级为口服给药C。
(1)下列患者慎用①哮喘或阻塞性肺病;②心脏传导异常;③胃肠道疾病或有溃疡性疾病史;④有癫痫史。
(2)慢性肝硬化患者本品清除时间减慢20%,但年龄与种族不影响药物代谢。
(3)哺乳期妇女使用可能对乳儿有危害。
(4)儿童使用的安全性和有效性未建立。
(1)与琥珀酰胆碱合用,由于协同效应,神经肌肉阻断的作用延长。
(2)与氨甲酰胆碱合用,胆碱能作用叠加,出现胆碱能不良反应(心动过缓、支气管痉挛、多汗、腹泻、呕吐)的风险增加。
(3)与酮康唑、伊曲康唑、红霉素等可抑制CYP3A4的药物,或与氟西汀、奎尼丁等可抑制CYP2D6的药物合用,本品的血浓度增加。
(4)与利福平、苯妥英钠、卡马西平等药酶诱导药合用,本品的血浓度降低。
(5)与洋地黄、华法林合用时要注意剂量。
盐酸多奈哌齐片:(1)5mg;(2)10mg。
盐酸多奈哌齐胶囊:5mg。
盐酸多奈哌剂口腔崩解片:5mg。
(1)取本品适量,加水溶解并稀释制成每1ml中约含20μg的溶液,照紫外-可见分光光度法(通则0401)测定,在230nm、271nm与316nm的波长处有最大吸收,在220nm、245nm与290nm的波长处有最小吸收。
(2)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(3)本品的红外光吸收图谱应与对照的图谱(光谱集1188图)一致。
(4)本品的水溶液显氯化物鉴别(1)的反应(通则0301)。以上(1)、(2)两项可选做一项。
酸度 取本品0.20g,加水10ml溶解后,依法测定(通则0631),pH值应为4.5~6.0。
溶液的澄清度与颜色 取本品0.20g,加水10ml溶解后,溶液应澄清无色;如显浑浊,与2号浊度标准液(通则0902第一法)比较,不得更浓。
溴化物 取本品1.0g,加水10ml,置水浴中微温使溶解,放冷,加盐酸3滴与三氯甲烷1ml,边振摇边滴加2%氯胺T溶液(临用新制)3滴,三氯甲烷层如显色,与标准溴化钾溶液(精密称取在105℃干燥至恒重的溴化钾0.1489g,加水溶解并稀释至100ml,摇匀,即得)1.0ml,用同一方法制成的对照溶液比较,不得更深(0.1%)。
有关物质照高效液相色谱法(通则0512)测定。
供试品溶液 取本品约10mg,置25ml量瓶中,加流动相溶解并稀释至刻度,摇匀。
对照溶液 精密量取供试品溶液1ml,置200ml量瓶中,用流动相稀释至刻度,摇匀。
灵敏度溶液 精密量取对照溶液2ml,置50ml量瓶中,用流动相稀释至刻度,摇匀。
色谱条件 用十八烷基硅烷键合硅胶为填充剂(4.6mm×150mm,5μm或效能相当的色谱柱);以1-癸烷磺酸钠2.5g溶于650ml水中,加乙腈350ml与高氯酸1ml混合均匀为流动相;检测波长为271nm;进样体积20μl。
系统适用性 要求主成分色谱峰的保留时间约为11分钟,理论板数按多奈哌齐峰计算不低于3000,多奈哌齐峰与相邻杂质峰之间的分离度应符合要求。灵敏度溶液色谱图中,主成分色谱峰的信噪比不小于10。
测定法 精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的2倍。
限度 供试品溶液色谱图中如有杂质峰,单个杂质峰面积不得大于对照溶液主峰面积的0.2倍(0.1%),各杂质峰面积的和不得大于对照溶液主峰面积(0.5%),小于灵敏度溶液主峰面积的峰忽略不计(0.02%)。
干燥失重 取本品,在105℃干燥至恒重,减失重量不得过0.5%(通则0831)。
炽灼残渣 取本品1.0g,依法检查(通则0841),遗留残渣不得过0.1%。
重金属 取炽灼残渣项下遗留的残渣,依法检查(通则0821第二法),含重金属不得过百万分之二十。
照高效液相色谱法(通则0512)测定。
供试品溶液 取本品约25mg,精密称定,置25ml量瓶中,加流动相溶解并稀释至刻度,摇匀,精密量取5ml,置50ml量瓶中,用流动相稀释至刻度,摇匀。
对照品溶液 取盐酸多奈哌齐对照品适量,精密称定,加流动相溶解并定量稀释制成每1ml中含0.1mg的溶液。
色谱条件见有关物质项下。进样体积10μl。
系统适用性要求除灵敏度要求外,见有关物质项下。
测定法 精密量取供试品溶液与对照品溶液,分别注入液相色谱仪,记录色谱图。按外标法以峰面积计算。
乙酰胆碱酯酶抑制剂。
遮光,密封,阴凉处保存。
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
