登录/
注册
登录/
注册
氯普噻吨
Lüpusaidun
Chlorprothixene
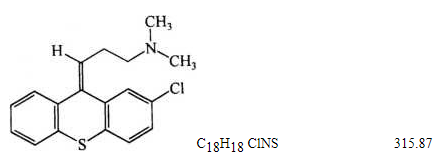
本品为(Z)-N,N-二甲基-3-(2-氯-9H-亚噻吨基)-1-丙胺。按干燥品计算,含C18H18ClNS不得少于98.0%。
本品为淡黄色结晶性粉末;无臭。
本品在三氯甲烷中易溶,在水中不溶。
熔点本品的熔点(通则0612)为96~99℃。
精神分裂症及躁狂症,以及伴有兴奋或情感症状的其他精神障碍。
(1)口服 ①成人治疗精神分裂症∶开始一次25~50mg,一日2~3次。然后根据临床需要与耐受程度增至一日400~600mg。②老年、体弱患者从小剂量开始,缓慢增至可耐受的较小的治疗用量。
(2)肌内注射 一次30mg,一日2~3次。
【儿科用法与用量】口服治疗精神分裂症6~12岁,一次10~25mg,一日3~4次。【儿科注意事项】此药抗精神病作用不如氯丙嗪,其镇静作用强。
(1)药效学 药理作用和机制类似氯丙嗪,抗精神病作用较氯丙嗪弱,镇静作用较强。其止吐和镇静作用在硫杂蒽类药物中较显著。
(2)药动学 口服后吸收快,达峰时间为1~3小时。主要在肝内代谢,大部分经尿排泄。半衰期为8~12小时。肌内注射后作用持续时间可达12小时以上。
(1)大量或增加药量时容易出现的不良反应有∶①低血压甚至晕倒;②肌肉僵直,颈背部尤为明显;③不停踱步;④双手或手指震颤或抖动;⑤头面、口部或颈部的肌肉抽搐等。
(2)比较少见的不良反应有∶①迟发性运动障碍;②皮疹或接触性皮炎。
(3)罕见的不良反应有∶①粒细胞减少症;②眼部细微沉积物;③黄疸等。
(1)基底神经节病变、帕金森病、帕金森综合征、骨髓抑制、青光眼、尿潴留、昏迷及对本品过敏者禁用。
(2)美国FDA妊娠期药物安全性分级为口服给药C。
(1)交叉过敏凡对吩噻嗪类、硫杂蒽类或其他药物过敏者,有可能对本品呈交叉过敏。
(2)妊娠及哺乳期内使用本品,对胎儿及婴儿的确切影响尚未肯定,在使用中应慎重。
(3)严重心血管或呼吸系统疾病患者慎用。
(4)对诊断的干扰可产生心电图改变如Q波与T波的变化,免疫妊娠试验可得假阳性反应,尿胆红素也呈假阳性。
(5)用药期间应定期随访检查∶①使用大量或持续治疗时,应定期检查白细胞计数;②肝功能检查;③有可疑黄疸时应检查尿胆红素;④长期用药者要定期做眼部检查,了解角膜与晶体有否沉积物。
(1)氯普噻吨能加强中枢抑制药例如吸入全麻药或巴比妥类等静脉全麻药的药效,合用时应将中枢抑制药的用量减少到常用量的1/4~1/2。
(2)同时并用抗酸药或泻药时,可减少氯普噻吨的吸收。
(3)氯普噻吨可降低惊厥阈值,因而使抗惊厥药作用减弱,不宜用于癫痫患者。
(4)与有抗胆碱作用的药物并用时,抗胆碱作用可加强。
(5)与肾上腺素并用,由于本品拮抗α受体,显示出肾上腺素激动β受体的效应,导致血压降低。
(6)与胍乙啶并用,可减低胍乙啶的抗高血压作用。
(7)与左旋多巴并用时,可抑制后者的抗帕金森病作用。
(8)三环类或单胺氧化酶抑制药与氯普噻吨并用,镇静及抗胆碱作用可更显著。
(9)氯普噻吨可掩盖某些抗生素的耳毒性。
氯普噻吨片∶(1)12.5mg;(2)15mg;(3)25mg;(4)50mg。
氯普噻吨注射液∶(1)2ml∶26.9mg;(2)2ml∶30mg。
(1)取本品约10mg,加硝酸2ml后,显亮红色,加水5ml稀释,置紫外光灯下检视,溶液显绿色荧光。
(2)取本品,加盐酸溶液(9→1000)制成每1ml中约含50µg的溶液,照紫外-可见分光光度法(通则0401)测定,在324nm的波长处有最大吸收。
(3)本品的红外光吸收图谱应与对照的图谱(光谱集304图)一致。
有关物质照高效液相色谱法(通则0512)测定。避光操作。
供试品溶液取本品约50mg,置50ml量瓶中,加乙腈10ml,超声使溶解,用流动相稀释至刻度,摇匀。
对照溶液精密量取供试品溶液1ml,置100ml量瓶中,用流动相稀释至刻度,摇匀。
色谱条件用十八烷基硅烷键合硅胶为填充剂;以磷酸盐溶液(取磷酸二氢钾6.0g、十二烷基硫酸钠2.9g、四丁基溴化铵9g,加水550ml溶解)-甲醇-乙腈(55∶5∶40)为流动相;检测波长为254nm;进样体积20µl。
系统适用性要求理论板数按氯普噻吨峰计算不低于2000,氯普噻吨峰与相邻杂质峰的分离度应符合要求。
测定法精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的2倍。
限度供试品溶液色谱图中如有杂质峰,单个杂质峰面积不得大于对照溶液主峰面积的2倍(2.0%),各杂质峰面积的和不得大于对照溶液主峰面积的3倍(3.0%)。
残留溶剂照残留溶剂测定法(通则0861第二法)测定。
供试品溶液取本品约0.5g,精密称定,置顶空瓶中,精密加N,N-二甲基甲酰胺5ml使溶解,密封。
对照品溶液取乙醇、乙酸乙酯、三氯甲烷与苯各适量,精密称定,用N,N-二甲基甲酰胺定量稀释制成每1ml中约含乙醇0.5mg、乙酸乙酯0.5mg、三氯甲烷6µg与苯0.2µg的混合溶液,精密量取5ml,置顶空瓶中,密封。
色谱条件以6%氰丙基苯基-94%二甲基聚硅氧烷(或极性相近)为固定液的毛细管柱为色谱柱;起始温度为50℃,维持15分钟,以每分钟30℃的速率升温至220℃,维持10分钟;进样口温度为160℃,检测器温度为250℃;顶空瓶平衡温度为85℃,平衡时间为30分钟。
系统适用性要求对照品溶液色谱图中,各成分峰之间的分离度均应符合要求。
测定法取供试品溶液与对照品溶液分别顶空进样,记录色谱图。
限度按外标法以峰面积计算,乙醇、乙酸乙酯、三氯甲烷与苯的残留量均应符合规定。
干燥失重取本品,置以五氧化二磷为干燥剂的干燥器中,在60℃减压干燥至恒重,减失重量不得过1.0%(通则0831)。
炽灼残渣取本品1.0g,依法检查(通则0841),遗留残渣不得过0.1%。
重金属取炽灼残渣项下遗留的残渣,依法检查(通则0821第二法),含重金属不得过百万分之二十。
取本品约0.25g,精密称定,加冰醋酸20ml溶解后,加结晶紫指示液1滴,用高氯酸滴定液(0.1mol/L)滴定至溶液显蓝色,并将滴定的结果用空白试验校正。每lml高氯酸滴定液(0.1mol/L)相当于31.59mg的C18H18ClNS。
抗精神病药。
遮光,密封保存。
氯普噻吨E-异构体

(Ε)-Ν,Ν-二甲基·3-(2-氯-9Η-亚嚏吨基)-1-丙胺
1、中华人民共和国药典:2020年版.四部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1599-5
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
