登录/
注册
登录/
注册
注射用丙氨酰谷氨酰胺
Zhusheyong Binganxian Guanxianan
Alanyl Glutamine for Injection
本品为丙氨酰谷氨酰胺的无菌冻干品或无菌粉末。按平均装量计算,含丙氨酰谷氨酰胺(C8H15N3O4)应为标示量的95.0%~105.0%。
本品为白色或类白色疏松块状物或粉末。
由于目前市售的其他复方氨基酸注射液不含谷氨酰胺,故本品主要用来补充其他氨基酸注射液的不足,为接受肠外营养的患者提供谷氨酰胺,包括处于分解代谢和高代谢状况者。
(1)用于改善消化道摄取、吸收不足或消化功能障碍引起的蛋白质营养不良,以及如消化道狭窄、梗阻、瘘、短肠综合征、消化液排泌或利用障碍,以及各种原因所致的长时间频繁剧烈呕吐或难治性腹泻、食欲缺乏或吞咽困难等。
(2)围手术禁食期营养支持。
(3)分解代谢旺盛疾病的营养支持,如大面积烧伤、严重创伤、危重感染等。
(4)经口虽能进食,但又必须限制食物通过消化道,减少肠道负荷,有利于病情缓解,如炎性肠病、消化道大出血等。
每日剂量:1.5~2.0ml/kg体重,相当于0.3~0.4gN(2)-L-丙氨酰-L谷氨酰胺(例如70kg体重患者每日需本品100~140ml)。
加入载体溶液时用量的调整:当氨基酸需要量为1.5g(kg·d)时,其中1.2g氨基酸由载体溶液提供,0.3g氨基酸由本品提供。当氨基酸需要量为2g(kg·d)时,其中1.6g氨基酸由载体溶液提供,0.4g氨基酸由本品提供。输注速度依载体溶液而定,但氨基酸不应超过0.1g(kg·h)。
【儿科用法与用量】静脉滴注一日300mg/kg。混合液中最大浓度不应超过3.5%。本品供给的氨基酸量不应超过全部氨基酸供给量的20%。
【儿科注意事项】(1)严重肝肾功能不全(每分钟肌酐清除率<25ml)或严重肝功能不全患儿禁用。
(1)药效学 谷氨酰胺是机体免疫细胞和黏膜细胞等快速生长细胞的主要能源,但其不能耐受高温高压的灭菌过程。而N(2)-L-丙氨酰-L-谷氨酰胺双肽可在体内分解为谷氨酰胺和丙氨酸的特性,使经由肠外营养输液补充谷氨酰胺成为可能。双肽分解释放出的氨基酸作为营养物质各自储存在身体的相应部位,并随机体的需要进行代谢。许多病症可出现体内谷氨酰胺的耗减,应用肠外营养支持时输注本品可阻遏这一情况的出现。
(2)药动学 本品输注后在体内迅速分解为谷氨酰胺和丙氨酸,其人体半衰期为2.4~3.8分钟(晚期肾功能不全患者为4.2分钟),血浆清除率为每分钟1.6~2.7L。此双肽的消失伴随等克分子数的游离氨基酸的增加。它的水解过程可能仅在细胞外发生。当输液量恒定不变时,通过尿液排泄的N(2)-L-丙氨酰-L-谷氨酰胺低于5%,与其他输注的氨基酸相同。
正确使用时,没有发现不良反应。当本品输注速度过快时,将出现寒战、恶心、呕吐,出现这种情况应立即停药。
严重肾功能不全(肌酐清除率<25ml/min)或严重肝功能不全的患者禁用。
(1)用前必须详细检查药液,如发现瓶身有破裂、漏气、变色浑浊、发霉、沉淀、变质等异常现象时绝对不应使用。开瓶药液一次用完,剩余药液切勿贮存再用。
(2)遇冷可能出现结晶,可将药液置50~60℃水浴中缓慢摇动,使结晶完全溶解并冷至37℃后再用。
(3)本品输液时必须缓慢,尤其当加入葡萄糖注射液而呈高渗状态,并由外周静脉输注时,必须严格控制滴注速度。
(4)本品含盐酸盐,大量输入可能导致酸碱失衡。大量应用或并用电解质输液时,应注意电解质与酸碱平衡。严重酸中毒患者慎用。
(5)将氨基酸溶液与其他液体或药物混合,会增加理化性不相容和微生物污染的危险。混合过程应在无菌条件下进行,并且混合物之间应是可配伍的。
(6)本品对妊娠期妇女怀孕期安全性的评估尚不明确,故仅在治疗益处明显大于危险性时才能给药。哺乳期妇女患者用药的安全性尚不明确,故哺乳期的妇女如果给药不可避免,则最好避免哺乳。
(7)对儿童安全性评价尚未确立(没有儿科使用经验)。
(8)由于高龄患者的生理功能通常减退,有必要对这些患者予以特殊关照,如减小剂量或减慢给药速度。
(9)密闭置暗处不超过25℃贮藏。
(10)对于代偿性肝功能不全的患者,建议定期监测肝功能。
(11)妊娠期妇女、哺乳期妇女和儿童使用本品的临床资料不足,故这类患者不推荐使用。
(12)应监测碱性磷酸酶、ALT、AST和酸碱平衡。
(1)取本品约20mg,加水1ml使溶解,加茚三酮试液5 滴,加热,即显蓝紫色。
(2)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
酸度 取本品1.0g,加水10ml 使溶解,依法测定(通则 0631),pH值应为5.4~6.0。
溶液的澄清度 取本品适量,加水溶解并制成每1ml中含0.20g的溶液,溶液应澄清无色;如显浑浊,与1号浊度标准液(通则0902第一法)比较,不得更浓。
吸光度 取本品,加水溶解并稀释制成每1ml中含0.2g 的溶液,照紫外-可见分光光度法(通则0401),在400nm的波长处测定,吸光度不得过0.05。
氨 照紫外-可见分光光度法(通则0401)测定。试验应在20~25℃进行。
供试品溶液 取本品适量,精密称定,加水溶解并定量稀释制成每1ml 中含 200mg的溶液,摇匀。
对照品溶液 取氯化铵29.7mg,精密称定,置500ml量瓶中,加水适量使溶解并稀释至刻度,摇匀(每1ml中相当于20μg的NH+4)。
测定法 精密量取还原酶I溶液(NADH)(取还原型辅酶I适量,用2-氧代戊二酸缓冲液制成每1ml中含0.2mg的溶液。该溶液4℃可保存3天)1.0ml,置吸收池中,加供试品溶液0.1ml和水1.9ml,混匀,反应5分钟。以水为参比,在340nm的波长处测定吸光度A1,再加入谷氨酸脱氢酶溶液(GLDH)(取谷氨酸脱氢酶适量,加水稀释制成每1ml中含1000单位的溶液)0.02ml,混匀,20分钟后测定吸光度A2。同法测定水和对照品溶液的吸光度,分别为B1、B2和C1、C2。按下式计算。
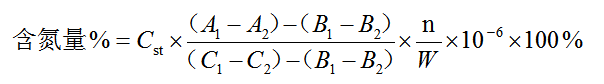
式中 Cst为对照品溶液的氨浓度,μg/ml;
n为供试品溶液的稀释倍数;
W为供试品的称样量。
限度 含氨不得过0.17%。
有关物质 照高效液相色谱法(通则0512)测定。
供试品溶液 取本品,精密称定,加流动相溶解并定量稀释制成每1ml中约含丙氨酰谷氨酰胺4mg的溶液。
对照品溶液 取主成分与各杂质对照品适量,分别精密称定,按下表的浓度加流动相溶解并定量稀释制成。

色谱条件、系统适用性要求与测定法 见丙氨酰谷氨酰胺有关物质项下。
限度 供试品溶液色谱图中如有杂质峰,按外标法以峰面积计算,各杂质含量与主成分标示量比较,含环-(L-丙氨酰-L-谷氨酰胺)不得过0.5%、含环-(L-丙氨酰-L-谷氨酸)不得过0.04%、含L-焦谷氨酰-L-丙氨酸不得过0.5%、含L-焦谷氨酸不得过0.2%、含D-丙氨酰-L-谷氨酰胺不得过0.25%、含L-丙氨酰谷氨酸不得过0.5%;其他单个未知杂质按外标法以丙氨酰谷氨酰胺峰面积计算,不得过0.5%,其他未知杂质总和不得过1.0%。
干燥失重 取本品,在105℃干燥至恒重,减失重量不得过1.0%(无菌粉末)或3.0%(无菌冻干品)(通则0831)。
细菌内毒素 取本品,依法检查(通则1143),每1mg中含内毒素的量应小于0.050EU。
无菌 取本品,用0.1%无菌蛋白胨水溶液适量溶解后,经薄膜过滤法处理,用0.1%无菌蛋白胨水溶液冲洗(每膜不少于100ml),以金黄色葡萄球菌为阳性对照菌,依法检查(通则1101),应符合规定。
其他 应符合注射剂项下有关的各项规定(通则0102)。
照高效液相色谱法(通则0512)测定。
供试品溶液 取装量差异项下的内容物,精密称取适量,加流动相溶解并定量稀释制成每1ml中约含丙氨酰谷氨酰胺0.05mg的溶液。
对照品溶液、系统适用性溶液、色谱条件、系统适用性要求与测定法 见丙氨酰谷氨酰胺含量测定项下。
(1)10g(2)20g
氨基酸类药。
密闭,在阴凉处保存。
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
