登录/
注册
登录/
注册
氢溴酸右美沙芬胶囊
Qingxiusuan Youmeishafen Jiaonang
Dextromethorphan Hydrobromide Capsules
本品含氢溴酸右美沙芬(C18H25NO・HBr・H2O)应为标示量的90.0%~110.0%。
本品内容物为白色粉末。
各种原因引起的干咳。
【成人用法与用量】口服 一次 10~20 mg,一日3~4次。
【儿科用法与用量】 口服 一次 2.5~5mg(2~6岁),一次5~10mg(6~12岁),一日3~4次。儿科注意事项:(1)2岁以下不宜使用。(2)宜用于无痰干咳年长儿。
(1)药效学 本品系中枢性镇咳药。抑制延髓咳嗽中枢而镇咳。其镇咳作用与可待因相等或稍强,无镇痛作用或成瘾性。
(2)药动学 服药后半小时起效,作用持续6小时。在肝脏代谢,血浆中右啡烷(dextrorphan)低,主要为3-甲氧吗啡烷、3-羟-17-甲吗啡烷及3-羟吗啡烷三种代谢产物。由肾脏排泄,包括原形物和脱甲基代谢物等。
偶有头晕、轻度嗜睡、口干、便秘、恶心和食欲缺乏。
美国FDA妊娠期用药安全性分级为口服给药C。
痰量多的患者慎用。
氢溴酸右美沙芬胶囊∶15mg。
(1)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(2)取本品内容物适量(约相当于氢溴酸右美沙芬0.15g),加水15ml使氢溴酸右美沙芬溶解,振摇,滤过,取滤液,显溴化物鉴别(1)的反应(通则0301)。
有关物质 照高效液相色谱法(通则0512)测定。
供试品溶液 取本品内容物适量,加流动相溶解并稀释制成每1ml中约含1.5mg的溶液。
对照溶液 精密量取供试品溶液1ml,置100ml量瓶中,用流动相稀释至刻度,摇匀。
灵敏度溶液 精密量取对照溶液1ml,置20ml量瓶中,用流动相稀释至刻度,摇匀。
系统适用性溶液、色谱条件、系统适用性要求与测定法 见氢溴酸右美沙芬有关物质项下。
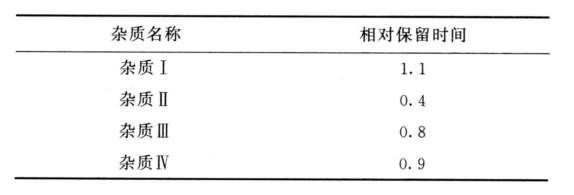
限度 供试品溶液色谱图中如有下表所示的杂质峰,除相对保留时间0.3之前的辅料峰外,杂质Ⅰ、Ⅱ、Ⅳ及乘以校正因子后的杂质Ⅲ(校正因子为0.2)的峰面积均不得大于对照溶液主峰面积(1.0%),且其峰面积(或校正后的峰面积)在对照溶液主峰面积0.5~1.0倍之间的杂质峰不得超过1个;其他单个杂质峰面积不得大于对照溶液主峰面积(1.0%),校正后各杂质峰面积的和不得大于对照溶液主峰面积的2倍(2.0%),小于灵敏度溶液主峰面积的色谱峰忽略不计。
含量均匀度 以含量测定项下测得的每粒含量计算,应符合规定(通则0941)。
溶出度 照溶出度与释放度测定法(通则0931第一法)测定。
溶出条件 以0.1mol/L盐酸溶液500ml为溶出介质,转速为每分钟100转,依法操作,经30分钟时取样。
供试品溶液 取溶出液适量,滤过,取续滤液。
对照品溶液 取氢溴酸右美沙芬对照品,精密称定,加溶出介质溶解并定量稀释制成每1ml中约含氢溴酸右美沙芬(按 C18H25NO・HBr・H2O计)30µg的溶液。
色谱条件 见含量测定项下。进样体积100µl。
系统适用性溶液与系统适用性要求 见含量测定项下。
测定法 精密量取供试品溶液与对照品溶液,分别注入液相色谱仪,记录色谱图,按外标法以峰面积计算每粒的溶岀量。
限度 标示量的85%,应符合规定。
其他 应符合胶囊剂项下有关的各项规定(通则0103)。
照高效液相色谱法(通则0512)测定。
供试品溶液 取本品10粒,分别将内容物倾入50ml量瓶中,囊壳用少量流动相分次洗净,洗液并入量瓶中,加流动相适量,超声使氢溴酸右美沙芬溶解,放冷,用流动相稀释至刻度,摇匀,滤过,取续滤液。
对照品溶液 取氢溴酸右美沙芬对照品适量,精密称定,加流动相溶解并定量稀释制成每1ml中含氢溴酸右美沙芬(按 C18H25NO・HBr・H2O计)0.3mg的溶液。
系统适用性溶液、色谱条件与系统适用性要求 见氢溴酸右美沙芬含量测定项下。
测定法 精密量取供试品溶液与对照品溶液,分别注入液相色谱仪,记录色谱图,按外标法以峰面积计算每粒的含量,并求得10粒的平均含量。
镇咳药。
遮光,密封保存。
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
