登录/
注册
登录/
注册
舒巴坦钠
Shubatanna
Sulbactam Sodium
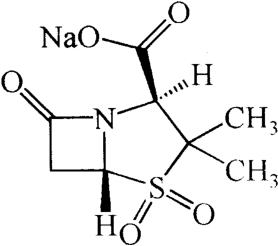
C8H10NNaO5S 255.22
本品为(2S,5R)-3,3-二甲基-7-氧代-4-硫杂-1-氮杂双环[3.2.0]庚烷-2-羧酸钠-4,4-二氧化物。按无水物计算,含舒巴坦(C8H11NO5S)不得少于88.6%。
本品为白色或类白色结晶性粉末;微有特臭。
本品在水中易溶,在甲醇中略溶,在乙醇中极微溶解,在丙酮或乙酸乙酯中几乎不溶。
比旋度 取本品,精密称定,加水溶解并定量稀释制成每lml中约含10mg的溶液,依法测定(通则0621),比旋度为+223°至+237°。
(1)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(2)本品的红外光吸收图谱应与对照的图谱(光谱集509图)一致。
(3)本品显钠盐鉴别(1)的反应(通则0301)。
溶液的澄清度与颜色 取本品5份,各0.30g,分别加水5ml溶解,溶液应澄清无色;如显浑浊,与1号浊度标准液(通则0902第一法)比较,均不得更浓;如显色,与黄色或黄绿色3号标准比色液(通则0901第一法)比较,均不得更深。
酸度 取本品,加水制成每1ml中约含50mg的溶液,依法测定(通则0631),pH值应为4.5~6.5。
有关物质 照高效液相色谱法(通则0512)测定。
供试品溶液 取本品适量,加流动相A溶解并稀释制成每1ml中约含2.5mg的溶液。
对照溶液 精密量取供试品溶液适量,用流动相A定量稀释制成每1ml中约含2.5μg的溶液。
系统适用性溶液 取舒巴坦钠约20mg,置50ml量瓶中,加水2ml及0.1mol/L氢氧化钠溶液0.5ml使溶解,室温放置10分钟,加0.1mol/L盐酸溶液0.5ml及6-氨基青霉烷酸溶液(0.015→50)1ml,用含量测定项下流动相稀释至刻度,摇匀。
色谱条件 用十八烷基硅烷键合硅胶为填充剂;流动相A为5.44g/L磷酸二氢钾溶液(用1mol/L磷酸溶液调节pH值至4.0),流动相B为乙腈,按下表进行线性梯度洗脱;检测波长为215nm;进样体积为20μl。

系统适用性要求 系统适用性溶液色谱图中,2-氨基-3-甲基-3-亚磺基丁酸、6-氨基青霉烷酸及舒巴坦依次出峰,舒巴坦峰的保留时间约为5~6分钟,2-氨基-3-甲基-3-亚磺基丁酸峰与6-氨基青霉烷酸峰之间的分离度应大于4.0,6-氨基青霉烷酸峰与舒巴坦峰间的分离度应大于6.0。
测定法 精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图。
限度 供试品溶液色谱图中如有杂质峰,2-氨基-3-甲基-3-亚磺基丁酸校正后的峰面积(乘以校正因子0.6)不得大于对照溶液主峰面积的5倍(0.5%);6-氨基青霉烷酸校正后的峰面积(乘以校正因子0.5)不得大于对照溶液主峰面积(0.1%);其他各杂质峰面积的和不得大于对照溶液主峰面积的8倍(0.8%),小于对照溶液主峰面积0.5倍的峰忽略不计。
2-乙基己酸 取本品,依法检查(通则0873),不得过0.5%。
水分 取本品,照水分测定法(通则0832第一法1)测定,含水分不得过1.0%。
重金属 取本品,依法检查(通则0821第一法),含重金属不得过百万分之二十。
可见异物 取本品5份,每份各2.0g,加微粒检查用水溶解,依法检查(通则0904),应符合规定。(供无菌分装用)
不溶性微粒 取本品适量,加微粒检查用水溶解并定量稀释制成每1ml中约含0.1g的溶液,静置10分钟后,依法测定(通则0903),每1g样品中,含10μm及10μm以上的微粒不得过6000粒,含25μm及25μm以上的微粒不得过600粒。(供无菌分装用)
细菌内毒素 取本品,依法检查(通则1143),每1mg舒巴坦中含内毒素的量应小于0.10EU。(供注射用)
无菌 取本品,用适宜溶剂溶解并稀释后,经薄膜过滤法处理,依法检查(通则1101),应符合规定。(供无菌分装用)
照高效液相色谱法(通则0512)测定。
供试品溶液 取本品适量,精密称定,加流动相溶解并定量稀释制成每1ml中约含舒巴坦0.7mg的溶液。
对照品溶液 取舒巴坦对照品适量,精密称定,加流动相溶解并定量稀释制成每1ml中约含舒巴坦0.7mg的溶液。
系统适用性溶液 见有关物质项下。
色谱条件 用十八烷基硅烷键合硅胶为填充剂;以5.44g/L磷酸二氢钾溶液(用lmol/L磷酸溶液调节pH值至4.0)-乙腈(98∶2)为流动相;检测波长为215nm;进样体积10μl。
系统适用性要求 系统适用性溶液色谱图中,舒巴坦峰与6-氨基青霉烷酸峰之间的分离度应大于4.0,舒巴坦峰的拖尾因子应不大于2.0。
测定法 精密量取供试品溶液与对照品溶液,分别注入液相色谱仪,记录色谱图。按外标法以峰面积计算供试品中C8H11NO5S的含量。
β-内酰胺酶抑制药。
严封,在阴凉干燥处保存。
(1)注射用舒巴坦钠 (2)注射用头孢哌酮钠舒巴坦钠 (3)注射用氨苄西林钠舒巴坦钠
中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
