登录/
注册
登录/
注册
坎地沙坦酯
Kandishatanzhi
Candesartan Cilexetil
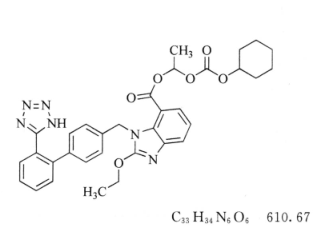
本品为(±)-1-[(环己氧基)羰基氧基]乙基 2-乙氧基-1-[[2’-(1 H-四氮唑基-5-基)联苯-4-基]甲基]-1H-苯并咪唑-7-羧酸酯。按干燥品计算,含C33H34N6O6不得少于 98.5%。
本品为白色或类白色结晶性粉末。
本品在三氯甲烷中易溶,在无水乙醇中微溶,在水中几乎不溶。
①高血压,可单独应用或与其他降压药如利尿药合用∶②心力衰竭。
口服(1)成人一次4~8mg,一日1次,由一日4mg开始,必要时增至一日12mg。
(2)严重肾功能不全宜从一次2mg,一日1次开始。肝功能不全,也宜从小剂量开始。
(1)药效学 坎地沙坦酯为一种前体药,在吸收过程中迅速、完全转化为活性代谢产物坎地沙垣。坎地沙坦为选择性血管紧张素Ⅱ1型受体(AT1)拮抗药,与AT1受体的结合力比氯沙坦高80倍,比氯沙坦活性代谢物EXP3174高10倍。
(2)药动学 坎地沙坦酯克服了坎地沙坦口服吸收差(15%)的缺点,生物利用度约42%,不受食物影响,可迅速、完全转化为坎地沙坦。口服后2~4小时达血药浓度峰值。在体内半衰期约9小时,在老年人似更长(9~11小时)。血浆蛋白结合率大于99%,大部分与白蛋白结合。主要经肾清除(60%),少部分通过胆汁排泄(40%)。肾功能轻度损伤的患者,无明显药物蓄积现象。肾功能严重损伤的患者,当本品用量达12mg时可能出现药物积聚现象。
(1)常见头晕。
(2)少见头痛、心悸、失眠、恶心、呕吐、胃部不适、腹泻、口腔炎、味觉异常,ALT升高、白细胞减少、肌酐升高、皮疹(如荨麻疹)、瘙痒等。
(1)重度肝损害和胆汁淤滞患者。
(2)美国FDA妊娠期药物安全性分级为口服给药C如在妊娠中,晚期用药D。
(1)下列情况慎用①双侧或单侧肾动脉狭窄患者。②肝功能损害者(可能进一步恶化)。③严重肾功能损害者(过度降压可能恶化肾功能)。④主动脉或二尖瓣狭窄,或肥厚型心肌病。⑤高钾血症。⑥严重低血压。⑦手术需全麻者。
(2)用药时检测①肾功能,包括电解质。给药后4周,以及调整剂量后2周复查血肌酐和血钾。肾功能不全患者,每次调整剂量前后监测血钾和肌酐;如肾功能恶化应及时停药一般每3~6个月监测肾功能。②监测血压,调整剂量初期应较频繁,包括必要时给药后24小时测卧位血压。
(3)儿童用药的安全性尚未明确。
(4)对高龄患者,宜根据其状态慎重用药,从小剂量开始。
(5)哺乳期妇女避免用本药,必须服药时应停止哺乳。
(6)本品过量时,可扩容纠正低血压,必要时透析治疗。
(1)与保钾利尿药,补钾药合用可出现高钾血症,特别当肾功能损害时。
(2)与利尿降压药合用,可能增强降压作用。
坎地沙坦酯片∶(1)2mg;(2)4mg;(3)8mg;(4)12mg;(5)16mg。
坎地沙坦酯胶囊∶(1)4mg;(2)8mg;(3)12mg。
(1)取有关物质项下的对照溶液作为供试品溶液;另取坎地沙坦酯对照品适量,加乙腈-水(3:2)溶解并稀释制成每 1ml 中约含 4μg 的溶液作为对照品溶液。照有关物质项下的色谱条件测定,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(2)本品的红外光吸收图谱应与对照的图谱(光谱集 1147 图)一致。
氯化物 取本品 0.40g,加水 100ml,强力振摇 10 分钟,滤过,取续滤液 25ml,依法检查(通则 0801),与标准氯化钠溶液 5.0ml 制成的对照液比较,不得更深(0.05%)。
照高效液相色谱法(通则 0512)测定。
溶剂 乙腈-水(3:2)。
供试品溶液 取本品约 20mg,置 50ml 量瓶中,加溶剂溶解并稀释至刻度,摇匀。
对照溶液 精密量取供试品溶液 1ml,置 100ml 量瓶中,用溶剂稀释至刻度,摇匀。
系统适用性贮备溶液 取供试品溶液 20ml,在 90℃水浴加热 2 小时后,放冷,加乙腈至 20ml。
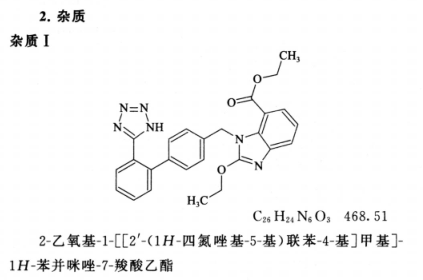
系统适用性溶液 取杂质 I 对照品适量,加溶剂溶解并稀释制成每 1ml 中约含 40μg 的溶液。取 2ml,置 20ml 量瓶中,用系统适用性贮备溶液稀释至刻度,摇匀。
灵敏度溶液 精密量取对照溶液适量,用溶剂定量稀释制成每 1ml 中约含坎地沙坦酯 0.2μg 的溶液。
色谱条件 用十八烷基硅烷键合硅胶为填充剂(Kromasil 100-5 C18 柱,4.6mm×250mm,5μm,或效能相当的色谱柱);以乙腈-冰醋酸-水(57:1:43)为流动相 A,乙腈-冰醋酸-水(90:1:10)为流动相 B,检测波长为 254nm。按下表进行梯度洗脱。进样体积为 10μl。

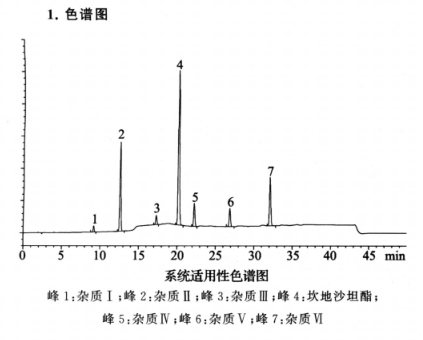
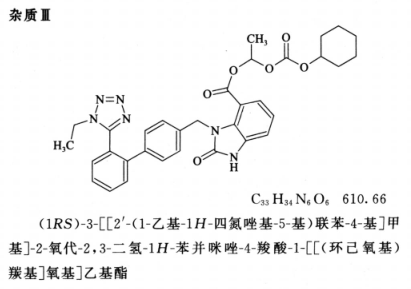
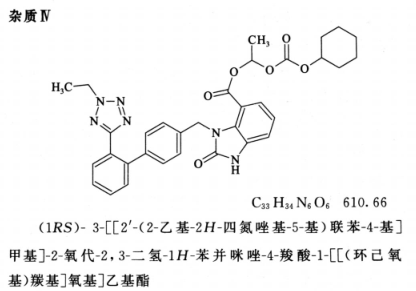
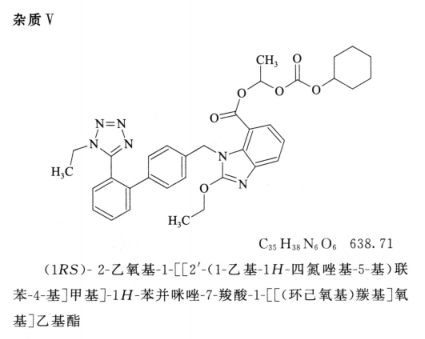
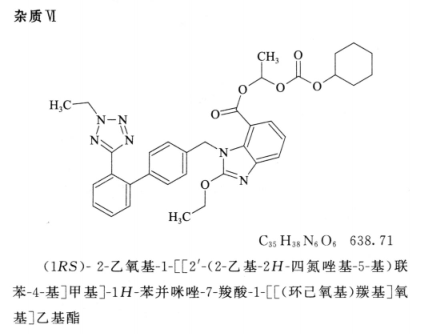
系统适用性要求 系统适用性溶液色谱图中,出峰顺序为杂质 I 峰、杂质 II 峰、杂质 Ⅲ 峰、坎地沙坦酯峰、杂质 IV 峰、杂质 V 峰与杂质 VI 峰;各峰间的分离度均应符合规定。灵敏度溶液色谱图中,坎地沙坦酯峰峰高的信噪比应大于 10。
测定法 精密量取供试品溶液和对照溶液,分别注入液相色谱仪,记录色谱图。
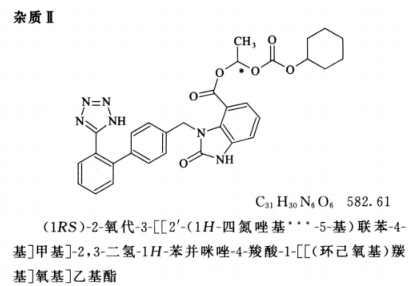
限度 供试品溶液色谱图中如有杂质峰,杂质 I 峰面积和杂质 VI 峰面积均不得大于对照溶液主峰面积的 0.2 倍(0.2%),杂质 Ⅱ 峰面积不得大于对照溶液主峰面积的 0.3 倍(0.3%),其他单个杂质峰面积不得大于对照溶液主峰面积的 0.1 倍(0.1%),各杂质峰面积的和不得大于对照溶液主峰面积的 0.6 倍(0.6%)。小于灵敏度溶液主峰面积的色谱峰忽略不计。
残留溶剂 照残留溶剂测定法(通则 0861 第二法)测定。
供试品溶液 取本品适量,精密称定,加二甲基亚砜溶解并定量稀释制成每 1ml 中约含 0.1g 的溶液,精密量取 5ml 置顶空瓶中,密封。
对照品溶液 取乙醇、二氯甲烷、甲苯与 N,N-二甲基甲酰胺各适量,精密称定,用二甲基亚砜定量稀释制成每 1ml 中含乙醇 0.5mg、二氯甲烷 60μg、甲苯 89μg 与 N,N-二甲基甲酰胺 8μg 的溶液,精密量取 5ml 置顶空瓶中,密封。
色谱条件 以 6%氰丙基苯基-94%二甲基聚硅氧烷(或极性相近)为固定液的毛细管柱为色谱柱;起始温度为 60℃,维持 8 分钟,以每分钟 35℃的速率升温至 150℃,维持 10 分钟;进样口温度为 200℃;检测器温度为 250℃;顶空瓶平衡温度为 95℃,平衡时间为 60 分钟。
系统适用性要求 对照品溶液色谱图中,各成分峰之间的分离度均应符合要求。
测定法 取供试品溶液与对照品溶液分别顶空进样,记录色谱图。
限度 按外标法以峰面积计算,乙醇、二氯甲烷、甲苯与 N,N-二甲基甲酰胺的残留量均应符合规定。
干燥失重 取本品 1.0g,在 105℃干燥至恒重,减失重量不得过 0.5%(通则 0831)。
炽灼残渣 取本品 1.0g,依法检查(通则 0841),遗留残渣不得过 0.1%。
重金属 取炽灼残渣项下遗留的残渣,依法检查(通则 0821 第二法),含重金属不得过百万分之十。
取本品约 0.45g,精密称定,加冰醋酸-醋酐(1:1)40ml,振摇使溶解,照电位滴定法(通则 0701),用高氯酸滴定液(0.1mol/L)滴定,并将滴定的结果用空白试验校正。每 1ml 高氯酸滴定液(0.1mol/L)相当于 61.07mg 的C33H34N6O6。
抗高血压药。
密封保存。
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
