登录/
注册
登录/
注册
尼索地平
Nisuodiping
Nisoldipine
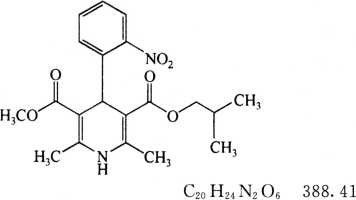
本品为(±)-2,6-二甲基-4-(2-硝基苯基)-1,4-二氢-3,5-吡啶二甲酸甲酯异丁酯。按干燥品计算,含C20H24N2O6不得少于98.5%。
本品为黄色结晶性粉末;无臭;遇光不稳定。
本品在丙酮或三氯甲烷中易溶,在乙醇中略溶,在水中几乎不溶。
熔点 本品的熔点(通则0612)为148~152℃。
①高血压,可单用或与其他降压药合用。②心绞痛。
口服 (1)治疗高血压 一次5~10mg,一日1次,可按血压每周逐渐调整剂量,可达一次40mg,一日1次。
(2)治疗心绞痛 一次10mg,开始一日1次,按症状逐渐调整至一次20~40mg,一日1次。
(1)药效学 本品为二氢吡啶类钙通道阻滞药,抑制钙跨过细胞膜进入血管平滑肌和心肌细胞。由于血管平滑肌的收缩过程依赖于细胞外钙离子通过特异性的离子通道进入细胞,抑制钙通道可以导致小动脉的扩张。体外研究显示,尼索地平对血管平滑肌作用具有选择性,即其对血管平滑肌的作用大于心肌。
(2)药动学 口服后尼索地平能被较好地吸收入血液循环,核素标记的药物87%在尿液和粪便中被检出。尼索地平的绝对生物利用度为5%。在服药后6~12小时血药浓度达峰值。终末消除半衰期为7~12小时。本品的血浆蛋白结合率很高,当血浆浓度在100 ng/ml~10gg/ml的范围时,未结合部分仅不到1%。尼索地平在体内经广泛代谢,在尿中已有5种代谢产物被发现。虽然口服进入体内的尼索地平中60%~80%经尿排泄,但尿中仅能发现微量的尼索地平原药。
(1)常见 头痛,浮肿,眩晕,颜面潮红,发热,心悸,肠胃不适(恶心,腹胀,便秘,腹泻)。
(2)少见 无力,肌痛,呼吸困难和心动过速。ALT、AST升高。
(3)罕见 胸痛、齿龈增生和男性乳房发育。
(1)心源性休克,怀孕与哺乳期妇女,对本品过敏者。
(2)美国FDA妊娠期药物安全性分级为口服给药C。
(1)哺乳期妇女宜慎用。
(2)个别患者开始治疗或合并饮酒,可能影响驾驶或操纵机器的能力。
(3)肝功能损害可增强和延缓本品作用,起始应小剂量并需仔细观察。
(4)过量可致低血压,亦可致心动过缓性心律失常。
(5)由于蛋白结合率高和分布容积大,本品不易为透析所清除。
(1)与β受体拮抗药或其他降压药合用有协同降压作用,应注意直立性低血压。
(2)与西咪替丁合用可使本品血药浓度增高,作用增强。
(3)奎尼丁可能使本品药-时曲线下面积(AUC)轻度减少,可能需要调整本品剂量。
(4)利福平由于诱导本品代谢酶的活力而加速本品代谢,因此减弱降压作用,需调整本品剂量。
(5)西柚汁可增强本品作用,不宜同时服用。
尼索地平片∶5mg。
尼索地平胶囊∶5mg。
(1)取本品约30mg,加丙酮2ml溶解,加20%氢氧化钠溶液3~5滴,振摇,溶液显橙红色。
(2)避光操作。取本品,加无水乙醇溶解并稀释制成每1ml中约含10μg的溶液,照紫外-可见分光光度法(通则0401)测定,在237nm的波长处有最大吸收。
(3)本品的红外光吸收图谱应与对照的图谱(光谱集1127图)一致。
有关物质 照高效液相色谱法(通则0512)测定。避光操作。
供试品溶液 取本品,精密称定,加流动相溶解并定量稀释制成每1ml中约含0.4mg的溶液。
对照溶液 取杂质I对照品与杂质Ⅱ对照品,精密称定,加流动相溶解并定量稀释制成每1ml中分别约含40μg的混合溶液,精密量取2ml,置100ml量瓶中,精密加入供试品溶液1ml,用流动相稀释至刻度,摇匀。
系统适用性溶液 取尼索地平、杂质I对照品与杂质Ⅱ对照品,加流动相溶解并稀释制成每1ml中分别约含400μg、1.2μg与1.2μg的混合溶液。
色谱条件 用十八烷基硅烷键合硅胶为填充剂;以甲醇-乙腈-水(50:15:35)为流动相;检测波长为237nm;进样体积10μl。
系统适用性要求 系统适用性溶液色谱图中,杂质I峰、杂质Ⅱ峰与尼索地平峰间的分离度均应符合要求。
测定法 精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的4倍。
限度 供试品溶液色谱图中如有与杂质I峰、杂质Ⅱ峰保留时间一致的色谱峰,按外标法以峰面积计算,均不得过0.2%;其他单个杂质峰面积不得大于对照溶液中尼索地平峰面积的0.5倍(0.5%);杂质总量不得过1.5%。
干燥失重 取本品,在105℃干燥至恒重,减失重量不得过0.5%(通则0831)。
炽灼残渣 取本品1.0g,依法检查(通则0841),遗留残渣不得过0.1%。
重金属 取炽灼残渣项下遗留的残渣,依法检查(通则0821第二法),含重金属不得过百万分之十。
取本品约0.25g,精密称定,加冰醋酸20ml及稀硫酸10ml,微温使溶解,放冷,加邻二氮菲指示液2滴,用硫酸铈滴定液(0.1mol/L)滴定至近终点时,在水浴中加热至50℃,继续缓缓滴定至橙红色消失,并将滴定的结果用空白试验校正。每1ml硫酸铈滴定液(0.1mol/L)相当于19.42mg的C20H24N2O6。
钙通道阻滞药。
遮光,密封保存。
杂质I
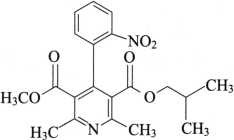
C20H22N2O6 386.40
2,6-二甲基-4-(2-硝基苯基)-3,5-吡啶二甲酸甲酯异丁酯
杂质Ⅱ
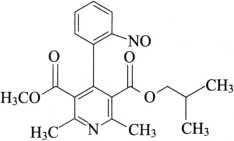
C20H22N2O5 370.40
2,6-二甲基-4-(2-亚硝基苯基)-3,5-吡啶二甲酸甲酯异丁酯
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
