登录/
注册
登录/
注册
盐酸普罗帕酮注射液
Yansuan Puluopatong Zhusheye
Propafenone Hydrochloride Injection
本品为盐酸普罗帕酮的灭菌水溶液。含盐酸普罗帕酮(C21H27NO3·HCl)应为标示量的90.0%~110.0%。
本品为无色的澄明液体。
静脉注射适用于阵发性室性心动过速、室上性心动过速及心房颤动(包括伴预激综合征者)。
静脉注射 成人按体重一次1~1.5mg/kg,或以70mg加5%葡萄糖液稀释,于10分钟内缓慢静脉注射,必要时10~20分钟后可重复一次。总量不超过210mg。以后可以每分钟0.5~1mg速度静脉滴注维持。
【儿科用法与用量】静脉注射20~40mg/h,严密监护。
【儿科注意事项】不良反应较少,主要有口干、舌唇麻木。
不良反应与剂量相关。
(1)心血管系统①可见心动过缓、心脏停搏及房室传导阻滞和室内阻滞,尤其原有窦房结或房室结功能障碍者、大量静脉持续应用者较易发生。应停药并静脉用阿托品或异丙肾上腺素。必要时起搏治疗。②有促心律失常作用,文献报道发生率4.7%,多见于有器质性心脏病者。静脉应用于心房扑动有传导比例减少而使心室率突然加快的报道。③4.4%产生低血压,尤其在原有心功能不全者,可用升压药、异丙肾上腺素等;也可加重或诱发心力衰竭,故对原有心力衰竭者应慎用。
(2)消化系统味觉异常为最常见不良反应,还可出现食欲缺乏、恶心、呕吐及便秘,也可产生口干及舌唇麻木。减药或停药可消失。
(3)神经系统头晕、目眩。减药或停药可消失。
(4)其他肝脏氨基转移酶升高,停药后2~4周恢复正常。
(1)窦房结功能障碍。
(2)二或三度房室传导阻滞,双束支传导阻滞(除非已有起搏器)。
(3)肝或肾功能障碍。
(4)美国FDA妊娠期药物安全性分级为口服给药C。
(1)不推荐用于有严重器质性心脏病的患者,特别是未控制的心功能不全和缺血。
(2)对诊断的干扰心电图P-R及Q-T间期延长,QRS波增宽。
(3)以下情况慎用①严重窦性心动过缓;②一度房室传导阻滞,束支传导阻滞,特别是新近出现者③低血压④肝或肾功能障碍。
(4)用药期间应注意随访检查①心电图②血压③心功能。
(5)本品血药浓度与剂量不成比例地增高,故在增量时应小心,以防血药浓度过高产生不良反应。
(6)静脉给药时须严密监测血压和心电图。
(1)其他抗心律失常药,包括维拉帕米、胺碘酮及奎尼丁等,可能增加本品不良反应。奎尼丁抑制肝的羟化代谢途径,使所有患者均变为慢代谢者。
(2)降压药可使本品的降压作用增强。
(3)本品在450mg/d时使地高辛血浓度升高35%,900mg/d时可升高85%。
(4)本品可增加普萘洛尔和美托洛尔的血浓度,但临床上未出现明显的不良反应。
(5)本品使华法林血浓度升高,共用时后者应调整剂量。
盐酸普罗帕酮注射液∶(1)5ml∶17.5mg;(2)5ml∶35mg; (3)10ml:35mg; (4)20ml:70mg。
(1)取本品5ml,置水浴上蒸干,残渣加乙醇4ml使溶解,加二硝基苯肼试液,振摇,即生成金黄色沉淀。
(2)取含量测定项下的溶液,照紫外-可见分光光度法(通则0401)测定,在210nm、248nm与304nm的波长处有最大吸收。
pH值 应为3.5~5.0(通则0631)。
有关物质 照高效液相色谱法(通则0512)测定。
供试品溶液 取本品,用流动相稀释制成每1ml中约含盐酸普罗帕酮1mg的溶液。
对照溶液 精密量取供试品溶液适量,用流动相定量稀释制成每1ml中约含2μg的溶液。
色谱条件、系统适用性要求与测定法 见盐酸普罗帕酮有关物质项下。
限度 供试品溶液色谱图中如有杂质峰,单个杂质峰面积不得大于对照溶液的主峰面积(0.2%),各杂质峰面积的和不得大于对照溶液主峰面积的2.5倍(0.5%)。
细菌内毒素 取本品,依法检查(通则1143),每1mg盐酸普罗帕酮中含内毒素的量应小于1.5EU。
其他 应符合注射剂项下有关的各项规定(通则0102)。
照紫外-可见分光光度法(通则0401)测定。
供试品溶液 精密量取本品,用乙醇定量稀释制成每1ml中约含盐酸普罗帕酮20μg的溶液。
测定法 取供试品溶液,在248nm的波长处测定吸光度,按C21H27NO3·HCl的吸收系数(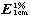 )为220计算。
)为220计算。
遮光,密闭保存。
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
