登录/
注册
登录/
注册
腺苷
Xiangan
Adenosine
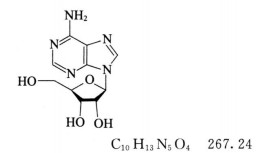
本品为6-氨基-9-β-D-呋喃核糖基-9H-嘌呤。按干燥品计算,含C10H13N5O4不得少于99.0%。
本品为白色或类白色结晶性粉末。
本品在热水中溶解,在水中微溶,在乙醇中极微溶解;在稀盐酸中易溶。
比旋度 取本品,精密称定,加1mol/L盐酸溶液溶解并定量稀释制成每1ml中约含25mg的溶液,在10分钟内依法测定(通则0621),比旋度为-45°至-49°。
静脉注射 成人①室上性心动过速∶首剂为6mg,在2秒内直接快速静脉注射,然后以氯化钠注射液快速冲洗。如心动过速未终止,可在1~2分钟后给第二剂和第三剂各12mg也可以先给初始剂量3mg,如心动过速仍然存在,可间隔1~2分钟给第二剂6mg,第三剂12mg。一次给药不超过12mg。②核素心肌血流显像∶按每分钟140μg/kg静脉给药,总量为0.84mg/kg,在6分钟内注射完。肾功能不全或肝功能不全患者无需调整剂量。
(1)药效学 腺苷是普遍存在于人体细胞的内源性核苷,主要由三磷酸腺苷降解形成,能产生短暂的负性肌力、传导和速率作用。其电生理作用包括降低窦房结和浦肯野纤维自律性、抑制房室结传导,使心房动作电位缩短并超极化、拮抗异丙肾上腺素对心室肌细胞动作电位的影响等。本品可产生一过性房室传导阻滞,因而能成功地终止房室结参与折返的阵发性室上性心动过速。本药对预激综合征旁路的前向传导无作用。窦房结和房室结对本药的生理剂量很敏感。通过本品对房室交界区的阻断是否出现暂时的房室分离,可用于宽QRS波心动过速的鉴别诊断。本品可引起一过性完全房室阻滞,能清楚地显示出室上性心律失常的心房活动,对诊断心房扑动、结内折返、心房颤动或多旁道传导有一定价值。另外,使用本品后正常冠状动脉的血流量增加,而狭窄冠状动脉的血流轻度增加或不增加,从而可增大正常动脉供血组织和狭窄动脉供血组织之间放射性核素分布的差异,故本药用于核素心肌血流灌注显像。
(2)药动学 本品在体内代谢迅速,起效快,作用时间短,一般仅10~20秒。主要由红细胞和血管内皮细胞摄取清除,清除半衰期<10秒。
本品快速注射后不良反应十分常见,但一般持续时间很短暂。
(1)心血管系统 一过性心动过缓、心脏停搏,可出现房性、房室交界性以及室性心律失常。可有心悸、高血压、低血压以及心绞痛样胸痛等。
(2)中枢神经系统常见头痛、眩晕、头昏、头部压迫感、感觉异常或神经过敏。少见癫痫。
(3)胃肠道胃肠道不适、腹痛、恶心、呕吐、味觉障碍(如金属味)等。
(4)泌尿生殖系统与剂量相关的一过性肾血流量减少。
(5)呼吸系统胸部紧缩感、呼吸困难、支气管痉挛、过度换气、咳嗽等,慢性阻塞性肺病患者可能出现呼吸衰竭。
(6)皮肤皮肤发红十分常见。可有明显颜面发红,烧灼感,大多数在数秒钟可缓解,可能与皮肤血管扩张有关。
(7)其他可有出汗、焦虑、视物模糊、手臂痛、背痛、颈痛,可引起过敏样反应。
(1)病态窦房结综合征,未置心脏起搏器者。
(2)二度或三度房室传导阻滞,未置心脏起搏器者。
(3)哮喘。
(4)心房颤动或心房扑动伴异常旁路。
(5)对本药过敏者。
(6)美国FDA妊娠期药物安全性分级为肠道外给药C。
(1)慎用于下列情况∶①高血压;②低血压;③心肌梗死;④不稳定型心绞痛。
(2)药物对哺乳的影响尚不明确。
(3)除可能改变房室传导外,本品不能将心房扑动、心房颤动或室性心动过速转为窦性心律。
(4)给药后,建议患者避免摄入咖啡。
(1)双嘧达莫可减少本药的代谢,增强药效,并引起不良反应如低血压、呼吸困难、呕吐等,因此如合用,应减小本品的剂量。
(2)本品与卡马西平合用,可加重心脏传导阻滞。
(3)本品的作用可被茶碱和其他甲基黄嘌呤类药物如咖啡因等拮抗,合用时可能需要增大本品剂量。
(4)地高辛、维拉帕米、奎尼丁、丙吡胺、胺碘酮对本药终止室上性心律失常的作用无明显影响。
腺苷注射液∶(1)2ml∶6mg;(2)30ml∶90mg(供诊断用)。
(1)取本品约10mg,加盐酸溶液(1→2)5ml溶解,加间苯三酚10mg,混匀,在水浴中加热5分钟,即显玫瑰红色。
(2)本品的红外光吸收图谱应与对照的图谱(光谱集886图)一致。
酸碱度 取本品0.25g,加水25ml,50℃水浴加热溶解后,放冷,依法检查(通则0631),pH值应为5.5~7.5。
溶液的澄清度与颜色 取本品,加水适量,50℃水浴溶解后,放冷,用水制成每1ml中含3mg的溶液,依法检查(通则0901第一法与通则0902第一法),溶液应澄清无色。
有关物质 照高效液相色谱法(通则0512)测定。
供试品溶液 取本品适量,精密称定,加水溶解并定量稀释制成每1ml中约含1mg的溶液。
对照溶液 精密量取供试品溶液1ml,用水定量稀释制成每1ml中约含1µg的溶液。
杂质对照品溶液 取腺嘌呤对照品适量,精密称定,加水溶解并定量稀释制成每1ml中约含1.0µg的溶液。
系统适用性溶液 取腺苷和腺嘌呤对照品各适量,置同一量瓶中,加水溶解并稀释制成每1ml中含腺苷和腺嘌呤各约0.2mg的溶液。
灵敏度溶液 取对照溶液1ml,置10ml量瓶中,用水稀释至刻度,摇匀。
色谱条件 用十八烷基硅烷键合硅胶为填充剂;以0.01mol/L磷酸二氢钾溶液(用2mol/L的氢氧化钾溶液调节pH值至5.7)-甲醇(85:15)为流动相;检测波长为260nm;进样体积20µl。
系统适用性要求 系统适用性溶液色谱图中,理论板数按腺苷峰计算不低于2000,腺苷峰与腺嘌呤峰之间的分离度应符合要求。灵敏度溶液色谱图中,主成分色谱峰峰高的信噪比应不小于20。
测定法 精密量取供试品溶液、对照溶液与杂质对照品溶液,分别注入液相色谱仪,记录色谱图至供试品溶液主成分峰保留时间的2倍。
限度 供试品溶液色谱图中如有与腺嘌呤杂质对照品溶液主峰保留时间一致的色谱峰,按外标法以峰面积计算,腺嘌呤含量不得过0.1%;其他单个杂质峰面积不得大于对照溶液的主峰面积(0.1%),其他杂质峰面积的和不得大于对照溶液主峰面积的3倍(0.3%),小于灵敏度溶液主峰面积的峰(0.01%)忽略不计。
残留溶剂 照残留溶剂测定法(通则0861第一法)测定。
供试品溶液 取本品约0.2g,精密称定,置10ml顶空瓶中,精密加水5ml,密封。
对照品溶液 取无水乙醇适量,精密称定,加水定量稀释制成1ml中含0.2mg的溶液,精密量取5ml,置10ml顶空瓶中,密封。
色谱条件 以100%聚乙二醇为固定液(或极性相近)的毛细管柱为色谱柱;柱温60℃;进样口温度为220℃;检测器温度220℃;顶空瓶平衡温度为90℃,平衡时间为30分钟。
测定法 取供试品溶液与对照品溶液分别顶空进样,记录色谱图。
限度 按外标法以峰面积计算,乙醇的残留量应符合规定。
氯化物 取本品1.0g,依法检查(通则0801),与标准氯化钠溶液7.0ml制成的对照液比较,不得更浓(0.007%)。
硫酸盐 取本品1.0g,依法检查(通则0802),与标准硫酸钾溶液2.0ml制成的对照液比较,不得更浓(0.02%)。
铵盐 取本品5.0g,依法检查(通则0808),与标准氯化铵溶液2.0ml制成的对照液比较,不得更深(0.0004%)。
干燥失重 取本品,在105℃干燥至恒重,减失重量不得过0.5%(通则0831)。
炽灼残渣 取本品1.0g,精密称定,缓缓炽灼至完全炭化,放冷,加硫酸1.5~2.0ml,依法检查(通则0841),遗留残渣不得过0.1%。
重金属 取炽灼残渣项下遗留的残渣,依法检查(通则0821第二法),含重金属不得过百万分之十。
取本品约0.2g,精密称定,加冰醋酸40ml,微热溶解,照电位滴定法(通则0701)用高氯酸滴定液(0.1mol/L)滴定,并将滴定结果用空白试验校正。每1ml高氯酸滴定液(0.1mol/L)相当于26.72mg的C10H13N5O4。
阵发性室上性心动过速治疗及冠状动脉疾病诊断药。
密封保存。
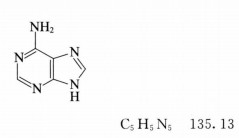
腺嘌呤(9H-嘌呤-6-胺)
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
