登录/
注册
登录/
注册
盐酸阿米洛利
Yansuan Amiluoli
Amiloride Hydrochloride
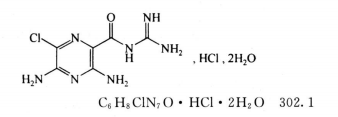
本品为N-脒基-3,5-二氨基-6-氯吡嗪-2-甲酰胺盐酸盐二水合物。按无水物计算,含C6H8ClN7O•HC1不得少于98.5%.
本品为淡黄色或黄绿色粉末;无臭或几乎无臭。
本品在水中微溶,在乙醇中极微溶解,在三氯甲烷或乙醚中几乎不溶。
水肿性疾病及难治性低钾血症的辅助治疗(由于螺内酯和氨苯蝶啶大部分需经肝脏代谢后排出体外,肝功能严重损害时,两药代谢减少,药物剂量不易控制,此时宜应用阿米洛利,因后者不需经肝脏代谢)。
口服 成人 开始一次2.5~5mg,一日1次,以后酌情调整剂量。一日最大剂量为20 mg。
(1)药效学 利尿作用于口服后2小时出现,6~10小时达高峰,可持续24小时。主要抑制末端远曲小管和集合管的Na+-K+和Na+-H+交换,从而Na+和水排出增多,而K+和H+排出减少。本药还使Ca2+和Mg2+排泄减少。本药与排钾利尿药合用,可明显减少钾的排泄,并部分减少Ca2+和Mg2+的排泄。而排Na+和水的作用则增强。其作用不依赖于醛固酮。
本药的促尿钠排泄和降压活性较弱,但与噻嗪类或袢利尿药合用有协同作用。本药 40 mg 与氨苯蝶啶200 mg的利尿作用相当,为目前潴钾利尿药中作用最强者。
(2)药动学 口服吸收不完全,生物利用度约为50%,食物可降低生物利用度。血浆蛋白结合率低,在体内不被代谢,t1/2为6~9小时。20%~50%经肾脏排泄,40%左右随粪便排出。
单独使用时高钾血症较常见。本药可引起高钾血症、低钠血症、高钙血症、轻度代谢性酸中毒;胃肠道反应如恶心、呕吐、食欲缺乏、腹痛、腹泻或便秘,头痛、头晕、直立性低血压、性功能下降;过敏反应表现为皮疹,甚至呼吸困难。
严重的反应有中性粒细胞减少(罕见)、再生障碍性贫血。
(1)对本药过敏者。
(2)肾功能减退(Cr>1.5mg/100 ml或BUN>30 mg/100 ml)者。
(3)高钾血症患者。
(4)留钾治疗(使用留钾药或补充钾)者。
(1)可引起高钾血症,如不纠正则可致死。高血钾常在与排钾利尿药合用时发生。肾功能损害、糖尿病患者发生率较高。应仔细监测每一名使用本药的患者。
(2)尚无实验证实本药能否经乳汁分泌。有证据显示该药可改变乳汁的分泌与组成,如果不能改用他药,应监测乳儿的不良反应以及是否摄入足够的乳汁。
(3)老年人应用本药较易出现高钾血症和肾功能损害等,用药期间应密切观察。
(4)对诊断的干扰 可使下列测定值升高:血糖(尤其是糖尿病患者),血肌酐和尿素氮(尤其是老年人和已有肾功能损害者),血钾、血镁及血浆肾素浓度。血钠浓度下降。
(5)下列情况慎用 ①无尿;②肾功能损害;③糖尿病;④糖尿病肾病;⑤电解质失衡和BUN增加;⑥代谢性或呼吸性酸中毒和低钠血症。
(6)美国FDA妊娠期用药安全性分级:口服给药B;D(如用于妊娠高血压)。
(1)与含碘造影剂合用,可增加发生急性肾功能衰竭的风险,给予造影剂之前应注意补足水分。
(2)与抗精神病药物合用,可增加发生直立性低血压的风险。
(3)与他克莫司合用,可发生致死性高血钾,肾功能不全者风险更大。
(4)与依普利酮或氨苯蝶呤等其他留钾利尿药合用,留钾的作用相加,引起高钾血症的风险增加,属禁忌。
盐酸阿米洛利片:2.5mg。
复方盐酸阿米洛利片:每片含盐酸阿米洛利2.5mg 和氢氯噻嗪 25 mg。
(1)取本品,加0.1mol/L盐酸溶液溶解并稀释制成每1ml中约含10µg的溶液,照紫外-可见分光光度法(通则0401)测定,在285nm与362nm的波长处有最大吸收。
(2)本品的红外光吸收图谱应与对照的图谱(光谱集828图)一致。
(3)取本品约20mg,加水20ml使溶解,滴加过量硝酸使沉淀完全,滤过,滤液显氯化物鉴别(1)的反应(通则0301)。
酸度 取本品0.10g,加水20ml溶解后,依法测定(通则0631),pH值应为3.8~5.2。
有关物质 照薄层色谱法(通则0502)试验。
供试品溶液 取本品,加甲醇溶解并定量稀释制成每lml中约含2mg的溶液。
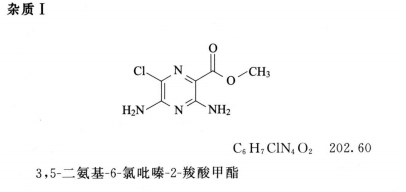
对照品溶液(1) 取杂质I对照品,精密称定,加甲醇溶解并定量稀释制成每1ml中约含10µg的溶液。
对照品溶液(2) 取杂质I对照品,精密称定,加甲醇溶解并定量稀释制成每1ml中约含4µg的溶液。
色谱条件 采用硅胶G薄层板,以二氧六环-稀氨溶液-水(90:6:6)为展开剂。
测定法 吸取上述三种溶液各10µ1,分别点于同一薄层板上,展开,晾干,置紫外光灯(365nm)下检视。
限度 供试品溶液如显与对照品溶液(1)相应的杂质斑点,其荧光强度与对照品溶液(1)的主斑点比较,不得更强;如显其他杂质斑点,与对照品溶液(2)的主斑点比较,不得更强。
水分 取本品,照水分测定法(通则0832第一法1)测定,含水分应为11.0%~13.0%。
炽灼残渣 取本品1.0g,依法检查(通则0841),遗留残渣不得过0.1%。
重金属 取炽灼残渣项下遗留的残渣,依法检查(通则0821第二法),含重金属不得过百万分之二十。
取本品约0.2g,精密称定,加0.01mol/L盐酸溶液5ml与乙醇50ml使溶解,照电位滴定法(通则0701),用氢氧化钠滴定液(0.1mol/L)滴定,两个突跃点体积的差作为滴定体积。每1ml的氢氧化钠滴定液(0.1mol/L)相当于26.61mg的C6H8ClN7O•HC1。
利尿药。
遮光,密封保存。
1、中华人民共和国药典:2020年版. 二部/国家药典委员会编. —北京:中国医药科技出版社,2020.5 ISBN 978-7-5214-1598-8
2、中华人民共和国药典临床用药须知:2015年版. 化学药和生物制品卷/国家药典委员会编.—北京:中国医药科技出版社,2017.9 ISBN 978-7-5067-9513-5
