登录/
注册
登录/
注册
儿童糖尿病
糖尿病(diabetesmellitus,DM)是由于胰岛素分泌绝对缺乏或相对不足所造成的糖、脂肪、蛋白质代谢紊乱症,分为原发性和继发性两类。原发性糖尿病又可分为:①1型糖尿病:由于胰岛β细胞破坏,胰岛素分泌绝对不足所造成,必须使用胰岛素治疗,故又称胰岛素依赖性糖尿病(insulindependentdiabetesmellitus,IDDM);②2型糖尿病:由于胰岛β细胞分泌胰岛素不足或靶细胞对胰岛素不敏感(胰岛素抵抗)所致,亦称非胰岛素依赖性糖尿病(noninsulin-dependentdiabetesmellitus,NIDDM);③青年成熟期发病型糖尿病(maturity-onsetdiabetesofyouth,MODY):是一种罕见的遗传性β细胞功能缺陷症,属常染色体显性遗传;④新生儿糖尿病:(neonataldiabetesmellitus,NDM)是指出生后6个月内发生的糖尿病,通常需要胰岛素治疗。多为单基因疾病,由于基因突变导致胰岛β细胞功能和成熟缺陷而致。新生儿糖尿病可分为永久性新生儿糖尿病(PNDM)和暂时性新生儿糖尿病(TNDM)。其中TNDM在新生儿期后会自行缓解或消失,但约有半数患者在儿童期或青少年期会再现。继发性糖尿病大多由一些遗传综合征(如21-三体综合征、Turner综合征和Klinefelter综合征等)和内分泌疾病(如Cushing综合征、甲状腺功能亢进症等)所引起。98%的儿童糖尿病为1型糖尿病,2型糖尿病甚少,但近年来随儿童肥胖症的增多而有增加趋势。
儿童1型糖尿病的发病率在各国之间差异较大,即使同一国家,不同民族或地区之间也不相同。芬兰(发病率36/10万)、意大利的撒丁岛(发病率36.4/10万)儿童(0~14岁)1型糖尿病发病率最高;其次为加拿大、瑞典、丹麦、美国和英国;韩国、日本及中国属低发病区,我国年发病率为1.04/10万。近年的流行病学研究表明,发病率逐年增高是世界的总趋势。4~6岁和10~14岁为1型糖尿病的高发年龄。本节主要叙述1型糖尿病。
1型糖尿病的确切发病机制尚未完全阐明。目前认为是在遗传易感基因的基础上由外界环境因素的作用引起的自身免疫反应,导致了胰岛β细胞的损伤和破坏。当90%以上的β细胞被破坏后,其残存的胰岛素分泌功能即不足以维持机体的生理需要,临床出现症状。遗传、免疫、环境等因素在1型糖尿病发病过程中都起着重要的作用。
1.遗传易感性 根据对同卵双胎的研究,1型糖尿病的患病一致性为50%,说明本病病因除遗传因素外还有环境因素作用,属多基因遗传病。通过对人类白细胞抗原(HLA)的研究发现,HLA的D区且类抗原基因(位于6p21.3)与本病的发生有关,已证明与HLA-DR3和DR4的关联性特别显著。还有研究认为HLA-DQβ链上第57位非门冬氨酸及HLA-DQα链上第52位的精氨酸的存在决定了1型糖尿病的易感性;反之HLA-DQβ57位门冬氨酸和HLA-DQα52位非精氨酸则决定1型糖尿病的保护性。但遗传易感基因在不同种族间有一定的差别,提示与遗传多态性有关。
2.环境因素 1型糖尿病的发病与病毒感染(如风疹病毒、腮腺炎病毒、柯萨奇病毒等)、化学毒物(如链尿菌素、四氧嘧啶等)、食物中的某些成分(如牛乳中的α、β-酪蛋白、乳球蛋白等)有关,以上因素可能会激发易感性基因者体内免疫功能的变化,产生β细胞毒性作用,最后导致1型糖尿病。
3.自身免疫因素 约90%的1型糖尿病患者在初次诊断时血中出现胰岛细胞自身抗体(ICA)、胰岛β细胞膜抗体(ICSA)、胰岛素自身抗体(IAA)以及谷氨酸脱羧酶(GAD)自身抗体、胰岛素受体自身抗体(IRA)等多种抗体,并已证实这些抗体在补体和T淋巴细胞的协同作用下具有对胰岛细胞的毒性作用。新近证实,细胞免疫异常对1型糖尿病的发病起着重要作用,树突状细胞源性细胞因子白介素-12会促进初始型CD4+T细胞(TH0)向I型辅助性T(TH1)细胞转化,使其过度活化而产生TH₁细胞类细胞因子,引起大量炎症介质的释放,进而损伤胰岛β细胞。
胰岛β细胞大都被破坏,分泌胰岛素明显减少,而分泌胰高糖素的细胞和其他细胞则相对增生。人体有6种主要涉及能量代谢的激素:胰岛素、胰高糖素、肾上腺素、去甲肾上腺素、皮质醇和生长激素。其中唯有胰岛素是促进能量储存的激素,其余5种激素在饥饿状态下均可促进能量释放,称为反调节激素。正常情况下,胰岛素可促进细胞内葡萄糖的转运,促进糖的利用和蛋白质的合成,促进脂肪合成,抑制肝糖原和脂肪的分解。糖尿病患儿的胰岛素分泌不足或缺如,使葡萄糖的利用减少,而反调节激素如胰高糖素、生长激素、皮质醇等增高,又促进肝糖原分解和葡萄糖异生作用,使脂肪和蛋白质分解加速,造成血糖和细胞外液渗透压增高,细胞内液向细胞外转移。当血糖浓度超过肾阈值(10mmol/L或180mg/dl)时即产生糖尿。自尿中排出的葡萄糖可达到200~300g/d,导致渗透性利尿,临床出现多尿症状,每日约丢失水分3~5L,钠和钾200~400mmol,因而造成严重的电解质失衡和慢性脱水。由于机体的代偿,患儿呈现渴感增强、饮水增多;因组织不能利用葡萄糖,能量不足而产生饥饿感,引起多食。胰岛素不足和反调节激素增高促进了脂肪分解,使血中脂肪酸增高,肌肉和胰岛素依赖性组织即利用这类游离脂肪酸供能以弥补细胞内葡萄糖不足,而过多的游离脂肪酸进入肝脏后,则在胰高糖素等生酮激素的作用下加速氧化,导致乙酰辅酶A增加,超过了三羧酸循环的氧化代谢能力,致使乙酰乙酸、β-羟丁酸和丙酮等酮体在体液中累积,形成酮症酸中毒。
酮症酸中毒时氧利用减低,大脑功能受损。酸中毒时CO₂严重潴留,为了排除较多的CO₂,呼吸中枢兴奋而出现不规则的深快呼吸,呼气中的丙酮产生特异的气味(腐烂水果味)。
1型糖尿病患者起病较急骤,多有感染或饮食不当等诱因。其典型症状为多饮、多尿、多食和体重下降(即“三多一少”)。但婴儿多饮、多尿不易被发觉,很快即可发生脱水和酮症酸中毒。儿童因为夜尿增多可发生遗尿。年长儿还可出现消瘦、精神不振、倦怠乏力等体质显著下降症状。约40%糖尿病患儿在就诊时即处于酮症酸中毒状态,这类患儿常因急性感染、过食、诊断延误、突然中断胰岛素治疗等因素诱发。多表现为起病急,进食减少,恶心,呕吐,腹痛,关节或肌肉疼痛,皮肤黏膜干燥,呼吸深长,呼气中带有酮味,脉搏细速,血压下降,体温不升,甚至嗜睡、淡漠、昏迷。常被误诊为肺炎、败血症、急腹症或脑膜炎等。少数患儿起病缓慢,以精神呆滞、软弱、体重下降等为主。
体格检查时除见体重减轻、消瘦外,一般无阳性体征。酮症酸中毒时可出现呼吸深长,带有酮味,有脱水征和意识障碍。病程较久,对糖尿病控制不良时可发生生长落后、智能发育迟缓、肝大,称为Mauriac综合征。晚期可出现蛋白尿、高血压等糖尿病肾病表现,最后致肾衰竭。还可出现白内障、视力障碍、视网膜病变,甚至失明。
儿童糖尿病有特殊的自然病程:
1.急性代谢紊乱期 从出现症状到临床确诊,时间多在1个月以内。约20%患儿表现为糖尿病酮症酸中毒;20%~40%为糖尿病酮症,无酸中毒;其余仅为高血糖、糖尿和酮尿。
2.暂时缓解期 约75%的患儿经胰岛素治疗后,临床症状消失、血糖下降、尿糖减少或转阴,即进入缓解期,也称“蜜月期”。此时胰岛β细胞恢复分泌少量胰岛素,对外源性胰岛素需要量减至0.5U/(kg·d)以下,少数患儿甚至可以完全不用胰岛素。这种暂时缓解期一般持续数周,最长可达半年以上。此期应定期监测血糖、尿糖水平。
3.强化期 经过缓解期后,患儿出现血糖增高和尿糖不易控制的现象,胰岛素用量逐渐或突然增多,称为强化期。在青春发育期,由于性激素增多等变化,增强了对胰岛素的拮抗,因此该期病情不甚稳定,胰岛素用量较大。
4.永久糖尿病期 青春期后,病情逐渐稳定,胰岛素用量比较恒定,称为永久糖尿病。
典型的病例诊断并不困难。对有口渴、消瘦、遗尿症状的患儿;或有糖尿病家族史者;或有不明原因脱水、酸中毒的患儿都应考虑本病的可能性,避免误诊。
本病应与下列情况相鉴别。
1.其他还原糖尿症 尿液中果糖和戊糖等其他还原糖均可使班氏试液呈色,用葡萄糖氧化酶法检测尿液可以鉴别。
2.非糖尿病性葡萄糖尿 有些先天性代谢病如Fanconi综合征、肾小管酸中毒、胱氨酸尿症或重金属中毒等患儿都可发生糖尿,主要依靠空腹血糖或葡萄糖耐量试验鉴别。
3.婴儿暂时性糖尿 病因不明,可能与患儿胰岛β细胞功能发育不够成熟有关。多在出生后6周内发病,表现为发热、呕吐、体重不增、脱水等症状。血糖增高,尿糖及酮体阳性,经补液等一般处理或给予小量胰岛素即可恢复。对这类患儿应进行葡萄糖耐量试验和长期随访,以与1型糖尿病鉴别。
4.其他发生酸中毒、昏迷的疾病 如尿毒症、感染中毒性休克、低血糖症、急腹症、颅内感染、重症肺炎等。
5.应激性高血糖症 多见于高热、严重感染、手术、呼吸窘迫、头部外伤后等的患者,系由应激诱发的一过性高血糖,不能诊断为糖尿病,但应注意长期随访。
1.尿液检查
(1)尿糖:定性一般阳性。尿糖可间接反映糖尿病患者血糖控制的状况。在用胰岛素治疗过程中,可监测尿糖变化,以判断饮食及胰岛素用量是否恰当。在空腹状态下先排空膀胱,半小时后排尿为“次尿”,相当于空腹时血糖的参考,从餐后至下次餐前一小时的尿为“段尿”,作为餐后血糖水平的参考。所得结果可粗略估计当时的血糖水平,利于胰岛素剂量的调整。
(2)尿酮体:糖尿病伴有酮症酸中毒时呈阳性。
(3)尿蛋白:监测尿微量白蛋白,可及时了解肾脏的病变情况。
2.血液检查
(1)血糖:符合下列任一标准即可诊断为糖尿病:
1)有典型糖尿病症状并且餐后任意时刻血糖水平≥11.1mmol/L。
2)空腹血糖(FPG)≥7.0mmol/L。
3)2小时口服葡萄糖耐量试验(OGTT)血糖水平≥11.1mmol/L。
空腹血糖受损(IFG):FPG为5.6~6.9mmol/L。糖耐量受损(IGT):口服1.75g/kg(最大75g)葡萄糖后2小时血糖在7.8~11.0mmol/L。IFG和IGT被称为“糖尿病前期”。
(2)血脂:血清胆固醇、甘油三酯和游离脂肪酸明显增加,适当的治疗可使之降低,故定期检测血脂水平,有助于判断病情控制情况。
(3)血气分析:酮症酸中毒在1型糖尿病患儿中发生率极高,当血气分析显示患儿血pH<7.30,HCO₃-<15mmol/L时,即有代谢性酸中毒存在。
(4)糖化血红蛋白:血红蛋白在红细胞内与血中葡萄糖或磷酸化葡萄糖呈非酶化结合,形成糖化血红蛋白(HbAlc),其量与血糖浓度成正相关。HbA1c可作为患儿在以往2~3个月期间血糖是否得到满意控制的指标。正常人HbA1c<7%,治疗良好的糖尿病患儿应<7.5%,HbA1c7.5%~9%提示病情控制一般,如>9%时则表示血糖控制不理想。
3.葡萄糖耐量试验本试验 用于空腹血糖正常或正常高限,餐后血糖高于正常而尿糖偶尔阳性的患儿。试验方法:试验当日自0时起禁食;清晨口服葡萄糖(1.75g/kg),最大量不超过75g,每克加水2.5ml,于3~5分钟内服完;口服前(0分钟)及口服后60分钟、120分钟和180分钟,分别测血糖。结果:正常人0分钟的血糖<6.7mmol/L,口服葡萄糖60分钟和120分钟后血糖分别低于10.0和7.8mmol/L;糖尿病患儿120分钟血糖值>11.1mmol/L。试验前应避免剧烈运动、精神紧张,停服双氢克尿噻、水杨酸等影响糖代谢的药物。
糖尿病是终生的内分泌代谢性疾病。其治疗目的是:消除高血糖引起的临床症状;积极预防并及时纠正酮症酸中毒;纠正代谢紊乱,力求病情稳定;使患儿获得正常生长发育,保证其正常的生活活动;预防并早期治疗并发症。
糖尿病治疗强调综合治疗,主要包括五个方面:合理应用胰岛素;饮食管理;运动锻炼;自我血糖监测;糖尿病知识教育和心理支持。糖尿病治疗必须在自我监测的基础上选择合适的胰岛素治疗方案和饮食管理、运动治疗等才能达到满意的效果。
1.糖尿病酮症酸中毒的治疗 酮症酸中毒迄今仍然是儿童糖尿病急症死亡的主要原因。对糖尿病酮症酸中毒必须针对高血糖、脱水、酸中毒、电解质紊乱和可能并存的感染等情况制订综合治疗方案。密切观察病情变化、血气分析和血、尿液中糖和酮体的变化,随时采取相应措施,避免医源性损害。DKA的即时评估与处理流程见图15-2。
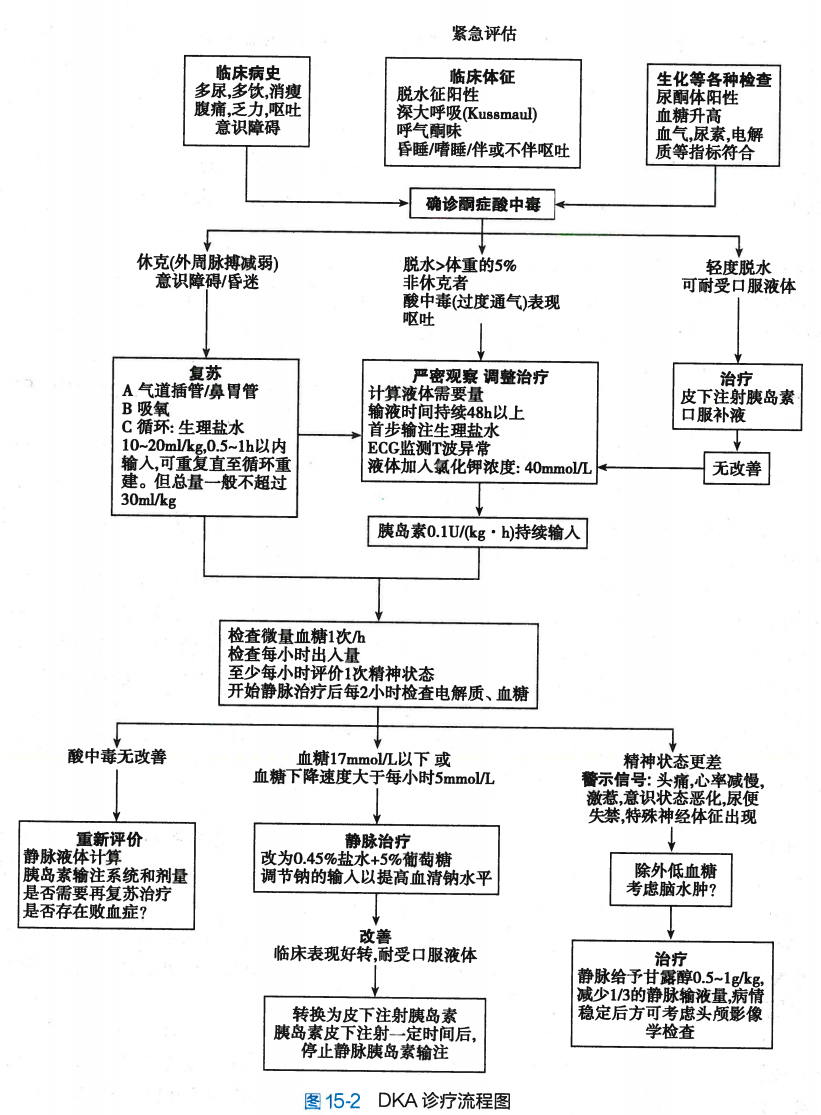
(1)液体治疗:主要针对脱水、酸中毒和电解质紊乱。酮症酸中毒时脱水量约为100ml/kg,一般均属等渗性脱水,应遵循下列原则输液。
快速补液:输液开始的第1小时,按20ml/kg(最大量1000ml)快速静滴生理盐水,以纠正血容量、改善血液循环和肾功能。第2~3小时,按10ml/kg静滴0.45%氯化钠溶液。当血糖<17mmol/L(300mg/dl)后,改用含有0.2%氯化钠的5%葡萄糖液静滴。
传统补液疗法建议在开始的12小时内至少补足累积损失量的一半。在此后的24小时内,可视情况按60~80ml/kg静滴同样溶液,以供给生理需要量和补充继续损失量。
目前国际上推荐48小时均衡补液法,即48小时均衡补入累积损失量及维持液,总液体张力约1/2张~2/3张。补液中根据监测情况调整补液中的离子浓度及含糖液等。
患儿在输液开始前由于酸中毒、分解代谢和脱水的共同作用使血清钾浓度增高,但总的体钾储备可能被耗竭。随着液体的输入,特别是应用胰岛素后,血钾迅速降低。因此,在患儿开始排尿后即应在输入液体中加入氯化钾溶液,一般按每日2~3mmol/kg(150~225mg/kg)补给,输入浓度不得>40mmol/L(0.3g/dl),并应监测心电图或血钾浓度。
酮症酸中毒时的酸中毒主要是由于酮体和乳酸的堆积,补充水分和胰岛素可以矫正酸中毒。为了避免发生脑细胞酸中毒和高钠血症,对酮症酸中毒不宜常规使用碳酸氢钠溶液,仅在血pH<7.1,HCO₃=<12mmol/L时,始可按2mmol/kg给予1.4%碳酸氢钠溶液静滴,先用半量,当血pH≥7.2时即停用,避免酸中毒纠正过快加重脑水肿。
在治疗过程中,应仔细监测生命体征、电解质、血糖和酸碱平衡状态,以避免在酮症酸中毒治疗过程中发生合并症,如脑水肿等。其表现为头痛、意识不清、嗜睡、痉挛、视盘水肿或脑疝等。
(2)胰岛素治疗:糖尿病酮症酸中毒时多采用小剂量胰岛素静脉滴注治疗。
对有休克的患儿,在补液治疗开始、休克逐渐恢复后才可应用胰岛素,以避免钾迅速从血浆进入细胞内,导致心律失常。
将胰岛素25U加入等渗盐水250ml中,按每小时0.1U/kg,自另一静脉通道缓慢匀速输入。每小时复查血糖,并根据血糖情况调整胰岛素输入量。血糖下降速度一般为每小时2~5mmol/L,胰岛素输注浓度一般不低于0.05U/(kg·h)。小剂量胰岛素静脉输注应持续至酮症酸中毒纠正(pH>7.3,血糖<12mmol/L),必要时可输入含糖的1/3~1/2张液体,以维持血糖水平为8~12mmol/L。当血糖<17mmol/L时,应将输入液体换成含0.2%氯化钠的5%葡萄糖液。只有当临床状况稳定后方可逐渐减少静脉输液,改为口服液体治疗,能进食后或在血糖下降至<11mmol/L、酮体消失时停用静脉注射胰岛素,改为胰岛素皮下注射,每次0.25~0.5U/kg,每4~6小时1次,直至血糖稳定为止。在停止滴注胰岛素前半小时即应皮下注射短效胰岛素0.25U/kg。
(3)控制感染:酮症酸中毒常并发感染,应在急救同时采用有效抗生素治疗。
酮症酸中毒在处理不当时,可引起脑水肿、低血糖、低血钾、碱中毒、心功能衰竭或肾衰竭等情况。因此在整个治疗过程中必须严密观察,随时调整治疗计划,避免因处理不妥而加重病情。
2.长期治疗措施
(1)饮食管理:糖尿病的饮食管理是进行计划饮食而不是限制饮食,其目的是维持正常血糖和保持理想体重。
1)每日总热能需要量:食物的热量要适合患儿的年龄、生长发育和日常活动的需要,每日所需热能(千卡)为1000+[年龄×(80~100)],对年幼儿宜稍偏高,而年龄大的患儿宜偏低。此外,还要考虑体重、食欲及运动量。全日热能分配为早餐1/5,中餐和晚餐分别为2/5,每餐中留出少量(5%)作为餐间点心。
2)食物的成分和比例:饮食中能源的分配为:蛋白质15%~20%,糖类50%~55%,脂肪30%。蛋白质成分在3岁以下儿童应稍多,其中一半以上应为动物蛋白,因其含有必需的氨基酸。禽类、鱼类、各种瘦肉类为较理想的动物蛋白质来源。糖类则以含纤维素高的,如糙米或玉米等粗粮为主,因为它们形成的血糖波动远较精制的白米、面粉或土豆等制品为小,蔗糖等精制糖应该避免。脂肪应以含多价不饱和脂肪酸的植物油为主。蔬菜选用含糖较少者。每日进食应定时,饮食量在一段时间内应固定不变。
(2)胰岛素治疗:胰岛素是糖尿病治疗能否成功的关键,但胰岛素治疗需要个体化,方案的选择依据年龄、病程、生活方式(如饮食、运动时间、上学)和既往健康状况等决定。胰岛素的种类、剂量、注射方法都与疗效有关。
1)胰岛素制剂(表15-7):目前胰岛素制剂有速效胰岛素类似物、短效胰岛素(RI)、中效珠蛋白胰岛素(NPH)、长效的鱼精蛋白锌胰岛素(PZI)、长效胰岛素类似物(甘精胰岛素和地特胰岛素)以及预混胰岛素等。
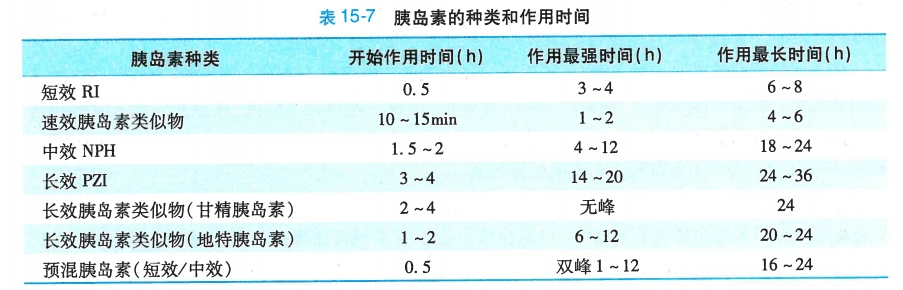
甘精胰岛素是在人胰岛素A链21位以甘氨酸替代天门冬氨酸,B链的羧基端加上两个精氨酸。地特胰岛素(detemir)是去掉B30位的氨基酸,在B29位点连接上含有14-C的脂肪酸链。其结构的改变使得该胰岛素稳定性增强,在酸性环境中呈溶解状态,即清澈溶液,注射前无需预先混匀,可直接皮下注射。一般1~2小时起效,作用时间维持24小时,每日只需注射1次。
2)胰岛素治疗方案:胰岛素的治疗方案很多,常用的有:①基础-餐时大剂量(basal-bolus)方案:即三餐前注射短效胰岛素或速效胰岛素类似物,睡前给予中效或长效胰岛素类似物。夜间的中长效胰岛素约占全日总量的30%~50%(一般先按30%计算),余量以速效或短效胰岛素分成3次于每餐前注射。但若以速效胰岛素类似物做餐前注射,则夜间使用基础胰岛素的比例要高一些。②持续皮下胰岛素输注(CSII)。可选用短效胰岛素或速效胰岛素类似物。将全日的总量分为基础量和餐前追加量两部分,两者的用量按1:1的比例分配。将24小时划分为日间(07:00~21:00)和夜间(21:00~次日07:00)两个阶段,日夜间基础量之比为2:1。餐前追加量按3餐平均分配,于每次餐前输注。在治疗过程中根据血糖或动态血糖监测结果进行基础率或餐前胰岛素剂量的动态调整。③每日3次注射方案:早餐前用短效(或速效)与中效胰岛素混合剂,午餐前单用短效(或速效)胰岛素,晚餐或睡前用短效(或速效)与中效胰岛素混合剂注射,或其他类似的方案。④每日2次注射方案:即短效(或速效)胰岛素与中效胰岛素的混合剂分别于早餐前和晚餐前2次注射。其中,短效(或速效)胰岛素与中效胰岛素的比例大约为1:2。早餐前胰岛素量为每日总量的2/3,晚餐前用量为总量的1/3。目前已较少应用。
3)胰岛素的剂量及其调整:胰岛素需要量婴儿偏小,年长儿偏大。新诊断的患儿,轻症患者胰岛素用量为每日0.5~1.0U/kg;青春期前儿童一般为每日0.75~1.0U/kg;青春期儿童每日用量通常>1.0U/kg。
早餐前注射的胰岛素提供早餐和午餐后的胰岛素,晚餐前注射的胰岛素提供晚餐后及次日晨的胰岛素。应根据用药日血糖或尿糖结果,调整次日的胰岛素用量,每2~3天调整剂量一次,直至尿糖不超过(++);血、尿糖稳定后,在相当时期中可不用再调整。
4)胰岛素注射笔:是普通注射器的改良,用喷嘴压力和极细针头推进胰岛素注入皮下,可减少皮肤损伤和注射精神压力。所用制剂为短效胰岛素、长效胰岛素以及中效胰岛素,其成分和比例随笔芯的不同而不同。皮下注射部位应选择大腿、上臂和腹壁等处,按顺序轮番注射,1个月内不要在同一部位注射2次,两针间距2.0cm左右,以防日久局部皮肤组织萎缩,影响疗效。注射部位参与运动时会加快胰岛素的作用,打球或跑步前不应在手臂和大腿注射,以免过快吸收引起低血糖。
5)胰岛素泵:能模拟正常胰腺的胰岛素分泌模式,持续24小时向患者体内输入微量胰岛素,更利于血糖的控制。胰岛素泵一般使用短效胰岛素或速效胰岛素类似物,但胰岛素使用剂量低于一般治疗方案。
长期佩戴胰岛素泵的患儿,应注意注射局部的消毒和保持清洁,并定期更换部位,以防感染。
6)胰岛素长期治疗过程中的注意事项:①胰岛素过量:胰岛素过量可致Somogyi现象,是由于胰岛素过量,在午夜至凌晨时发生低血糖,在反调节激素作用下使血糖升高,清晨出现高血糖,即出现低血糖-高血糖反应。如未及时诊断,因日间血糖增高而盲目增加胰岛素用量,可造成恶性循环。故对于尿量增加,同时有低血糖出现或一日内血糖波动较大,胰岛素用量大于每日1.5U/kg者,应怀疑Somogyi现象,可测午夜后1~3时血糖,以及时诊断。②胰岛素不足:胰岛素不足可致黎明现象(dawnphenomenon)。因晚间胰岛素不足,在清晨5~9时呈现血糖和尿糖增高,可加大晚间注射剂量或将NPH注射时间稍往后移即可。持久的胰岛素用量不足可使患儿长期处于高血糖状态,症状不能完全消除,导致生长停滞、肝脾大、高血糖、高血脂,容易发生酮症酸中毒巴。③胰岛素耐药:患儿在无酮症酸中毒情况下,每日胰岛素用量>2U/kg仍不能使高血糖得到控制时,在排除Somogyi现象后称为胰岛素耐药。可换用更纯的基因重组胰岛素。
(3)运动治疗:运动时肌肉对胰岛素的敏感性增高,从而增强葡萄糖的利用,有利于血糖的控制。运动的种类和剧烈程度应根据年龄和运动能力进行安排,有人主张1型糖尿病的学龄儿童每天都应参加1小时以上的适当运动。运动时必须做好胰岛素用量和饮食调节,运动前减少胰岛素用量或加餐,固定每天的运动时间,避免发生运动后低血糖。
(4)宣教和管理:由于儿童糖尿病的病情不稳定,易于波动,且本病需要终生饮食控制和注射胰岛素,给患儿及其家庭带来种种精神负担。因此,医生、家长和患儿应密切配合。医务人员必须向患儿及家长详细介绍有关知识,帮助患儿树立信心,使其能坚持有规律的生活和治疗,同时加强管理制度,定期随访复查。出院后家长和患儿应遵守医生的安排,接受治疗。同时做好家庭记录,包括饮食、胰岛素注射次数和剂量、血糖监测情况等。
(5)血糖监测:血糖监测记录有助于分析治疗效果及引起低血糖的原因,利于指导胰岛素调整以降低血糖波动水平,也有助于防止糖尿病急性并发症酮症酸中毒以及低血糖的发生。血糖监测包括日常血糖监测和定期总体血糖监测。
日常血糖监测包括自我血糖监测和连续血糖监测(CGM)。自我血糖监测记录应包括:血糖水平、胰岛素剂量、影响血糖控制的特殊事件(患病、聚会、运动、月经等)、低血糖事件及其严重程度,以及潜在的日常生活习惯改变等。连续血糖监测(CGM)是指将含有传感器的导管或小塑胶片插入皮下,连续监测组织间液血糖,血糖传感器可将血糖水平数据传输至接收器或胰岛素泵。CGM有助于了解饮食、胰岛素方案以及运动对血糖的影响,并及时指导其调整;可发现隐匿性高血糖/低血糖以及血糖异常持续的时间,有助于及时调整胰岛素治疗方案。
定期总体血糖监测建议患者每3~6个月定期至医院进行糖化血红蛋白、肝肾功能等检查。HbA1c可反映过去2~3个月的平均血糖水平,但不能反映血糖波动程度和低血糖事件。
(6)预防慢性并发症:儿童青少年1型糖尿病作为终生性疾病,慢性并发症的早期筛查和预防非常重要,控制血糖、血压和血脂及改善微循环是控制慢性并发症的有效手段。青春期前发病的糖尿病患者,发病5年后或满11岁或至青春期,每年筛查一次糖尿病肾病、糖尿病视网膜病变等慢性并发症;青春期发病的糖尿病患者发病2年后每年筛查一次各项并发症,年龄达到12岁的患者应进行血脂的监测。
