登录/
注册
登录/
注册
慢性髓系白血病
CML在我国年发病率为(0.39~0.99)/10万。在各年龄组均可发病,国内中位发病年龄45~50岁,男性多于女性。起病缓慢,早期常无自觉症状。病人可因健康检查或因其他疾病就医时才发现血象异常或脾大而被确诊。
(一)慢性期(CP)
CP一般持续1~4年。病人有乏力、低热、多汗或盗汗、体重减轻等代谢亢进的症状,由于脾大而自觉有左上腹坠胀感。常以脾大为最显著体征,往往就医时已达脐或脐以下,质地坚实,平滑,无压痛。如果发生脾梗死,则脾区压痛明显,并有摩擦音。肝脏明显肿大较少见。部分病人胸骨中下段压痛。当白细胞显著增高时,可有眼底充血及出血。白细胞极度增高时,可发生白细胞淤滞症。
1.血象 白细胞数明显增高,常超过20×109/L,可达100×10⁹/L以上,血片中粒细胞显著增多,可见各阶段粒细胞,以中性中幼、晚幼和杆状核粒细胞居多;原始(I+Ⅱ)细胞<10%;嗜酸性、嗜碱性粒细胞增多,后者有助于诊断。血小板可在正常水平,近半数病人增多;晚期血小板渐减少,并出现贫血。
2.中性粒细胞碱性磷酸酶(NAP) 活性减低或呈阴性反应。治疗有效时NAP活性可以恢复,疾病复发时又下降,合并细菌性感染时可略升高。
3.骨髓象 骨髓增生明显至极度活跃,以粒细胞为主,粒红比例明显增高,其中中性中幼、晚幼及杆状核粒细胞明显增多,原始细胞<10%。嗜酸性、嗜碱性粒细胞增多。红细胞相对减少。巨核细胞正常或增多,晚期减少。偶见Gaucher样细胞。
4.细胞遗传学及分子生物学检查 95%以上的CML细胞中出现Ph染色体(小的22号染色体),显带分析为t(9;22)(q34;q11)。9号染色体长臂上C-ABL原癌基因易位至22号染色体长臂的断裂点簇集区(BCR)形成BCR-ABL融合基因。其编码的蛋白主要为P210,P210具有酪氨酸激酶活性。Ph染色体可见于粒、红、单核、巨核及淋巴细胞中。不足5%的CML有BCR-ABL融合基因阳性而Ph染色体阴性。
5.血液生化检查 血清及尿中尿酸浓度增高。血清LDH增高。
(二)加速期(AP)
AP可维持几个月到数年。常有发热、虚弱、进行性体重下降、骨骼疼痛,逐渐出现贫血和出血;脾持续或进行性肿大;对原来治疗有效的药物包括酪氨酸激酶抑制剂(tyrosinekinaseinhibitor,TKI)无效;外周血或骨髓原始细胞≥10%;外周血嗜碱性粒细胞>20%;不明原因的血小板进行性减少或增笔记加;Ph染色体阳性细胞中又出现其他染色体异常,如:+8、双Ph染色体、17号染色体长臂的等臂[i(17q)]等。
(三)急变期(BC)
为CML的终末期,临床与AL类似。多数急粒变,少数为急淋变或急单变,偶有图核细胞及红细胞等类型的急性变。急性变预后极差,往往在数个月内死亡。外周血或骨髓中原始细胞>20%或出现髓外原始细胞浸润。
凡有不明原因的持续性白细胞数增高,根据典型的血象、骨髓象改变,脾大,Ph染色体阳性或BCR-ABL融合基因阳性即可作出诊断。Ph染色体尚可见于1%AML、5%儿童ALL及25%成人ALL,应注意鉴别。不具有Ph染色体和BCR-ABL融合基因而临床特征类似于CML的疾病归入骨髓增生异常综合征/骨髓增殖性肿瘤。其他需要鉴别的疾病如下。
1.其他原因引起的脾大 血吸虫病、慢性疟疾、黑热病、肝硬化、脾功能亢进等均有脾大。但各病均有各自原发病的临床特点,并且血象及骨髓象无CML的典型改变。Ph染色体及BCR-ABL融合基因均阴性。
2.类白血病反应 常并发于严重感染、恶性肿瘤等基础疾病,并有相应原发病的临床表现。粒细胞胞质中常有中毒颗粒和空泡。嗜酸性粒细胞和嗜碱性粒细胞不增多。NAP反应强阳性。Ph染色体及BCR-ABL融合基因阴性。血小板和血红蛋白大多正常。原发病控制后,白细胞恢复正常。
3.骨髓纤维化 原发性骨髓纤维化脾大显著,血象中白细胞增多,并出现幼粒细胞等,易与CML混淆。但骨髓纤维化外周血白细胞数一般比CML少,多不超过30×109/L。NAP阳性。此外幼红细胞持续出现于外周血中,红细胞形态异常,特别是泪滴状红细胞易见。Ph染色体及BCR-ABL融合基因阴性。病人可存在JAK2V617F、CALR、MPL基因突变。多次多部位骨髓穿刺干抽。骨髓活检网状纤维染色阳性。
CML治疗应着重于慢性期早期,避免疾病转化,力争细胞遗传学和分子生物学水平的缓解,一旦进入加速期或急变期(统称进展期)则预后不良。
CMLCP的治疗如下。
(一)高白细胞血症紧急处理
需合用羟基脲和别嘌醇。对于白细胞计数极高或有白细胞淤滞症表现的CP病人,可以行治疗性白细胞单采。明确诊断后,首选伊马替尼。
(二)分子靶向治疗
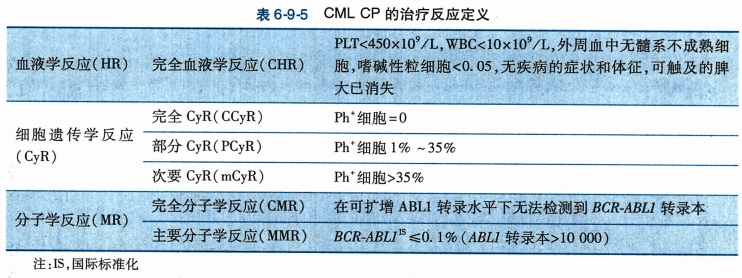
第一代酪氨酸激酶抑制剂(TKI)甲磺酸伊马替尼(imatinibmesylate,IM)为2-苯胺嘧啶衍生物,能特异性阻断ATP在ABL激酶上的结合位置,使酪氨酸残基不能磷酸化,从而抑制BCR-ABL阳性细胞的增殖。IM治疗CML病人完全细胞遗传学缓解率92%,10年总体生存率(overallsurvival,OS)可达84%。IM耐药与基因点突变、BCR-ABL基因扩增和表达增加、P糖蛋白过度表达有关,随意减停药物容易产生BCR-ABL激酶区的突变,发生继发性耐药。第二代TKI如尼洛替尼(nilotinib)、达沙替尼(dasatinib)治疗CML能够获得更快、更深的分子学反应,逐渐成为CML一线治疗方案的可选药物。TKI治疗期间可发生白细胞、血小板减少和贫血的血液学毒性以及水肿、头痛、皮疹、胆红素升高等非血液学毒性。在开始TKI治疗后的第3个月,6个月,12个月,18个月进行疗效监测,对判定为治疗失败的病人需进行ABL激酶区基因突变检查,并根据突变形式以及病人对药物的反应更换TKI或考虑造血干细胞移植。服药的依从性以及严密监测对于获得最佳疗效非常关键。CML治疗反应定义详见表6-9-5。
(三)干扰素
干扰素(interferon-α,IFN-α)是分子靶向药物出现之前的首选药物。目前用于不适合TKI和allo-HSCT的病人。常用剂量300万~500万U/(m²·d),皮下或肌内注射,每周3~7次,坚持使用,推荐和小剂量阿糖胞苷(cytarabine,Ara-C)合用,Ara-C常用剂量10~20mg/(m²·d),每个月连用10天。CCyR率约13%,但有效者10年生存率可达70%,约50%的有效者可以获得长期生存。主要副作用包括乏力、发热、头痛、食欲缺乏、肌肉骨骼酸痛等流感样症状和体重下降、肝功能异常等,可引起轻到中度的血细胞减少。预防性使用对乙酰氨基酚等能够减轻流感样症状。
(四)其他药物治疗
1.羟基脲(hydroxyurea,HU) 细胞周期特异性化疗药,起效快,用药后两三天白细胞计数即下降,停药后又很快回升。常用剂量为3g/d,分2次口服,待白细胞减至20×10⁹/L左右时,剂量减半。降至10×109/L时,改为小剂量(0.5~1g/d)维持治疗。需经常检查血象,以便调节药物剂量。耐受性好,单独应用HU的CP病人中位生存期约为5年。单独应用HU目前限于高龄、具有合并症、TKI和IFN-α均不耐受的病人以及用于高白细胞淤滞时的降白细胞处理。
2.其他药物 包括Ara-C、高三尖杉酯碱(homoharringtonine,HHT)、砷剂、白消安等。
(五)异基因造血干细胞移植(allo-HSCT)
Allo-HSCT是CML的根治性治疗方法,但在CML慢性期不作为一线选择。Allo-HSCT仅用于移植风险很低且对TKI耐药、不耐受以及进展期的CML病人。
进展期CML的治疗如下。
AP和BC统称为CML的进展期。CML进入进展期之后,需要评估病人的细胞遗传学、分子学BCR-ABL水平以及BCR-ABL激酶区的突变。AP病人,如果既往未使用过TKI治疗,可以采用加量的一代或者二代TKI(甲磺酸伊马替尼600~800mg/d或尼洛替尼800mg/d或达沙替尼140mg/d)使病人回到CP,立即行allo-HSCT治疗。BC病人,明确急变类型后,可以在加量的TKI基础上,加以联合化疗方案使病人回到CP后,立即行allo-HSCT治疗。Allo-HSCT干细胞来源不再受限于全相合供体,可以考虑行单倍型相合亲缘供体移植。移植后需辅以TKI治疗以减少复发,并可以行预防性供体淋巴细胞输注以增加移植物抗白血病效应。移植后复发可以用供体淋巴细胞输注联合或不联合TKI治疗以求再缓解。
进展期CML总体预后不佳,明显不如CP的移植效果,TKI可以改善移植预后。有报道TKI联合allo-HSCT治疗进展期CML,3年0S达59%。
除allo-HSCT外,进展期CML还可采用单用TKI,联合化疗,干扰素治疗或其他治疗,疗效有限且不能持久。
TKI出现前,CMLCP病人中位生存期为39~47个月,3~5年内进入BC终末期,少数病人CP可延续10~20年。影响CML预后的因素包括:病人初诊时的风险评估;疾病治疗的方式;病情的演变。干扰素治疗的OS较化疗有所提高,对干扰素的反应对预后有预示作用。TKI应用以来,生存期显著延长。
