登录/
注册
登录/
注册
15.1 试验项目
15.1.1 动物实验
15.1.1.1 体重
15.1.1.2 双歧杆菌
15.1.1.3 乳杆菌
15.1.1.4 肠球菌
15.1.1.5 肠杆菌
15.1.1.6 产气荚膜梭菌
15.1.2 人体试食试验
15.1.2.1 双歧杆菌
15.1.2.2 乳杆菌
15.1.2.3 肠球菌
15.1.2.4 肠杆菌
15.1.2.5 拟杆菌
15.1.2.6 产气荚膜梭菌
15.2 试验原则
15.2.1 动物实验和人体试食试验所列指标均为必做项目。
15.2.2 正常动物或肠道菌群紊乱模型动物任选其一。
15.2.3 受试样品中含双歧杆菌、乳杆菌以外的其它益生菌时,应在动物和人体试验中加测该益生菌。
15.2.4 在进行人体试食试验时,应对受试样品的食用安全性作进一步的观察。
15.3 结果判定
15.3.1 动物实验:符合以下任一项,可判定该受试样品有助于调节肠道菌群动物实验结果阳性。
15.3.1.1 双歧杆菌和/或乳杆菌(或其它益生菌)明显增加,梭菌减少或无明显变化,肠球菌、肠杆菌无明显变化。
15.3.1.2 双歧杆菌和/或乳杆菌(或其它益生菌)明显增加,梭菌减少或无明显变化,肠球菌和/或肠杆菌明显增加,但增加的幅度低于双歧杆菌、乳杆菌(或其它益生菌)增加的幅度。
15.3.2 人体试食试验:符合以下任一项,可判定该受试样品具有有助于调节肠道菌群的作用。
15.3.2.1 双歧杆菌和/或乳杆菌(或其它益生菌)明显增加,梭菌减少或无明显变化,肠球菌、肠杆菌、拟杆菌无明显变化。
15.3.2.2 双歧杆菌和/或乳杆菌(或其它益生菌)明显增加,梭菌减少或无明显变化,肠球菌和/或肠杆菌、拟杆菌明显增加,但增加的幅度低于双歧杆菌、乳杆菌(或其它益生菌)增加的幅度。
1 动物实验
1.1 实验动物
推荐用近交系小鼠,18-22g,单一性别,每组10-15只。
1.2 剂量分组及受试样品给予时间
实验设三个剂量组和一个阴性对照组,以人体推荐量的10倍为其中的一个剂量组,另设二个剂量组,必要时设阳性对照组。受试样品给予时间14天,必要时可以延长至30天。
1.3 实验步骤
在给予受试样品之前,无菌采取小鼠肛门内粪便0.1g,10倍系列稀释,选择合适的稀释度分别接种在各培养基上。培养后,以菌落形态、革兰氏染色镜检、生化反应等鉴定计数菌落,计算出每克湿便中的菌数,取对数后进行统计处理。最后一次给予受试样品之后24h,与实验前同样方式取直肠粪便,检测肠道菌群,方法同上。
1.4 观察指标
体重、双歧杆菌、乳杆菌、肠球菌、肠杆菌、产气荚膜梭菌。
1.5 数据处理和结果判定
资料可用方差分析,但需按方差分析的程序先进行方差齐性检验,方差齐,计算F值,F值<F0.05,结论:各组均数间差异无显著性;F值≥F0.05,P≤0.05,用多个实验组和一个对照组间均数的两两比较方法进行统计;对非正态或方差不齐的数据进行适当的变量转换,待满足正态或方差齐要求后,用转换后的数据进行统计;若变量转换后仍未达到正态或方差齐的目的,改用秩和检验进行统计。
比较实验前后自身及组间双歧杆菌、乳杆菌、肠球菌、肠杆菌、产气荚膜梭菌的变化情况,实验组实验前后自身比较差异有显著性,或实验后实验组与对照组组间比较差异有显著性、且实验组实验前后自身比较差异有显著性,符合以下任一项,可以判定该受试样品动物实验结果阳性。
1.5.1 粪便中双歧杆菌和/或乳杆菌明显增加,产气荚膜梭菌减少或不增加,肠杆菌、肠球菌无明显变化。
1.5.2 粪便中双歧杆菌和/或乳杆菌明显增加,产气荚膜梭菌减少或不增加,肠杆菌和/或肠球菌明显增加,但增加的幅度低于双歧杆菌/乳杆菌增加的幅度。
2 人体试食试验
2.1 受试者纳入标准
2.1.1 一个月内未患过胃肠疾病者。
2.1.2 一个月内未服用过抗生素者。
2.2 受试者排除标准
2.2.1 年龄在65岁以上者,妊娠或哺乳期妇女,过敏体质及对本保健食品过敏者。
2.2.2 合并有心血管、脑血管、肝、肾和造血系统等严重疾病及内分泌疾病,精神病患者。
2.2.3 停服受试样品或中途加服其它药物,无法判断功效或资料不全者。
2.2.4 短期内服用与受试功能有关的物品,影响到对结果的判断者。
2.3 试验设计及分组要求
采用自身和组间两种对照设计。按受试者的菌群状况随机分为试食和对照组,尽可能考虑影响结果的主要因素如年龄、性别、饮食因素等,进行均衡性检验,以保证组间的可比性。每组受试者不少于50例。
2.4 受试样品的剂量和使用方法
试食组按推荐服用方法、服用量服用受试产品,对照组可服用安慰剂或采用空白对照。受试样品给予时间14天,必要时可以延长至30天。试验期间不改变原来的饮食习惯,正常饮食。
2.5 观察指标
2.5.1 安全性指标:
2.5.1.1 一般状况包括精神、睡眠、饮食、大小便、血压等
2.5.1.2 血、尿、便常规检查
2.5.1.3 肝、肾功能检查(仅在试验开始前检查一次)
2.5.1.4 胸片、心电图、腹部B超检查(仅在试验开始前检查一次)
2.5.2 功效性指标:双歧杆菌、乳杆菌、肠球菌、肠杆菌、拟杆菌、产气荚膜梭菌。
2.6 试验步骤:在给予受试样品之前,无菌采取受试者粪便1.0g,10倍系列稀释,选择合适的稀释度分别接种在各培养基上。培养后,以菌落形态、革兰氏染色镜检、生化反应等鉴定计数菌落,计算出每克湿便中的菌数,取对数后进行统计处理。最后一次给予受试样品之后24h,再次检测,方法同上。
2.7 数据处理和结果判定
试验数据为计量资料,可用t检验进行分析。凡自身对照资料可以采用配对t检验,两组均数比较采用成组t检验,后者需进行方差齐性检验,对非正态分布或方差不齐的数据进行适当的变量转换,待满足正态方差齐后,用转换的数据进行t检验;若转换数据仍不能满足正态方差齐要求,改用t’检验或秩和检验;但变异系数太大(如CV>50%)的资料应用秩和检验。
符合以下任一项,且试验组试食前后自身比较及试食后试食组与对照组比较,差异均有显著性,可以判定该受试样品具有有助于调节肠道菌群的作用。
2.7.1 粪便中双歧杆菌和/或乳杆菌明显增加,产气荚膜梭菌减少或不增加,肠杆菌、肠球菌、拟杆菌无明显变化。
2.7.2 粪便中双歧杆菌和/或乳杆菌明显增加,产气荚膜梭菌减少或不增加,肠杆菌和/或肠球菌、拟杆菌明显增加,但增加的幅度低于双歧杆菌/乳杆菌增加的幅度。
附:肠道菌群检验用培养基和培养方法(动物和人体通用)
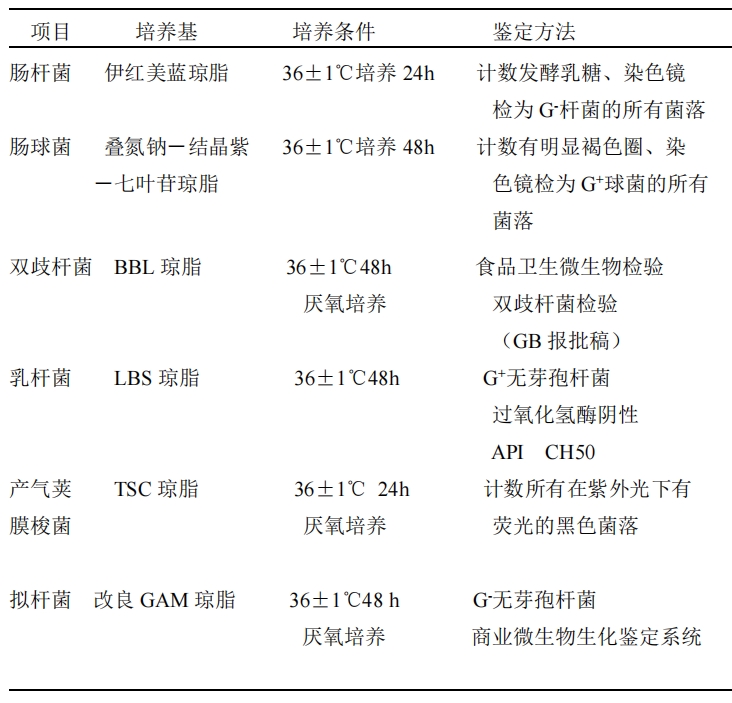
培养基成分和制法
肠杆菌培养基(伊红美蓝琼脂EMB)

制法:
将蛋白胨、磷酸盐和琼脂溶解于蒸馏水中,调整pH,分装于烧瓶内,121℃高压灭菌15min备用。临用时加入乳糖并加热溶化琼脂,冷却至50~55℃,加入伊红和美蓝溶液,摇匀,倾注平板。
肠球菌培养基(叠氮钠-结晶紫-七叶苷琼脂)

制法:
将上述成分溶解于蒸馏水中,调整pH,分装后,121℃高压灭菌15min备用。
拟杆菌选择性培养基(改良GAM琼脂)

制法:
1、将上述成分溶解于蒸馏水中,调整pH,分装后,115℃高压灭菌15min,冷却至50℃左右,加入混合抗生素1mL/L,0.1%维生素K1溶液1mL/L,氯化血红素2.5mL/L,脱纤维兔血70mL/L,混匀后倾注平板。
2、混合抗菌素的配制:将卡那霉素100mg、新霉素100mg、万古霉素1mg装入小瓶内,加入1mL无菌蒸馏水,充分溶解后,备用。
产气荚膜梭菌选择性培养基(TSC琼脂)

制法:
将各成分溶于蒸馏水中,调整pH至7.6,121℃高压灭菌10min,冷却至50℃左右,每250mL基础溶液中加入20mLD-环丝氨酸溶液,混匀后倾注平板。
D-环丝氨酸溶液配制:溶解1gD-环丝氨酸于200mL蒸馏水,膜过滤除菌后,于4℃冷藏保存备用。
双歧杆菌选择性培养基(BBL琼脂)
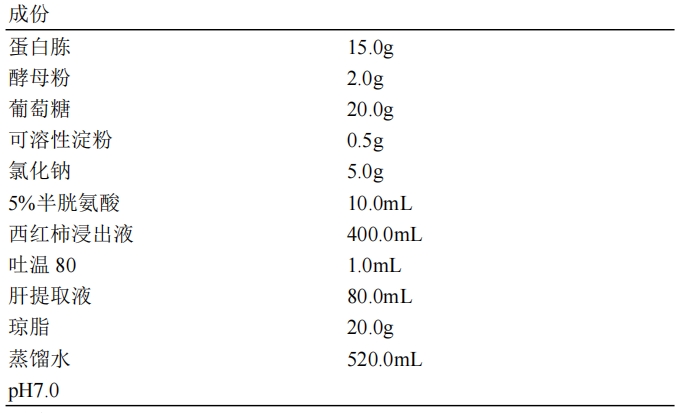
制法:
西红柿浸出液的制备:将新鲜西红柿洗净称重后切碎,加等量蒸馏水在100℃水浴中加热,时时搅拌,约90min,然后用绒布过滤,校正pH7.0,分装三角瓶,115℃高压灭菌15-20min。
肝提取液的制备:称取新鲜猪肝1000g,切成小块或绞碎,加蒸馏水至2000mL,混匀,置冰箱中过夜。第二天煮沸15-20min,绒布过滤,并挤压收集全部滤液,加水补足原量。分装三角瓶,115℃高压灭菌15-20min。
将上述成分配制,调整pH7.0,分装三角瓶,115℃高压灭菌15-20min。
乳杆菌选择性培养基(LBS琼脂)
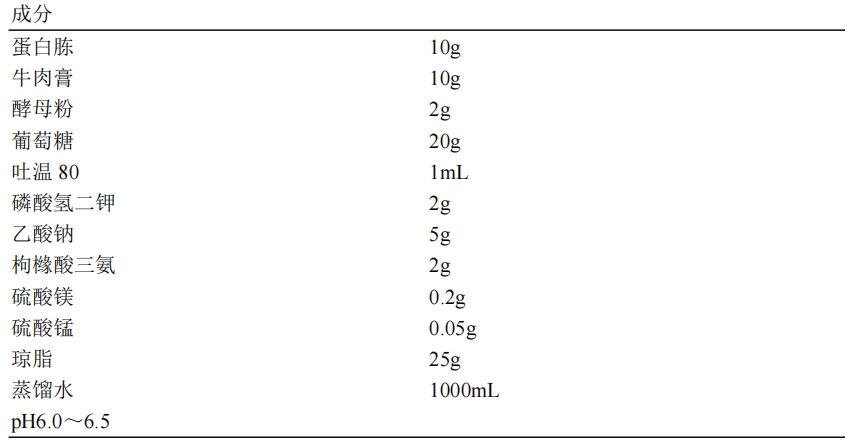
制法:
将上述成分溶解于蒸馏水中,调整pH,分装于烧瓶内,115℃高压灭菌15-20min备用。
稀释液
0.5%L-半胱氨酸 0.5mL
吐温 801.0mL
酵母粉 0.5g
蒸馏水 1000mL
pH7.0-7.2
115℃高压灭菌20min备用。
